Chapitre 2
Bilan
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétence : Travailler en autonomie.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
1Les deux principaux composants de l'air
Le saviez-vous ?
L'air est composé d'environ \dfrac{1}{5} de dioxygène et de \dfrac{4}{5} de diazote.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
2Une méthode de séparation des composants de l'air
- L'air est en réalité composé de nombreux gaz : diazote, dioxygène, dioxyde de carbone, vapeur d'eau, argon, etc.
- On peut liquéfier l'air en abaissant sa température. Cela permet de le stocker plus facilement.
- L'industrie sépare les constituants de l'air par distillation. Chaque gaz est récupéré quand sa température d'ébullition est atteinte. Pur, le gaz isolé peut alors être à nouveau liquéfié si nécessaire.
Le saviez-vous ?
La distillation est une technique utilisant une vaporisation suivie d'une liquéfaction, et qui permet la séparation des constituants d'un mélange. Le liquide obtenu est appelé le « distillat ».
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
3L'air possède une masse
Le saviez-vous ?
Dans les conditions normales de température et de pression (0 °C et 1 013 hPa), la masse d'un litre d'air est de 1,3 g.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
4Ce qui fait varier la masse de l'air
Le saviez-vous ?
Les variations de composition de l'air peuvent modifier la masse habituelle d'un litre d'air.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- La compression : activité 2.
- Les conditions normales de température et de pression : activité 4.
- La corrosion du fer : activité 1.
- La détente : activité 2.
- La distillation : activité 2.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
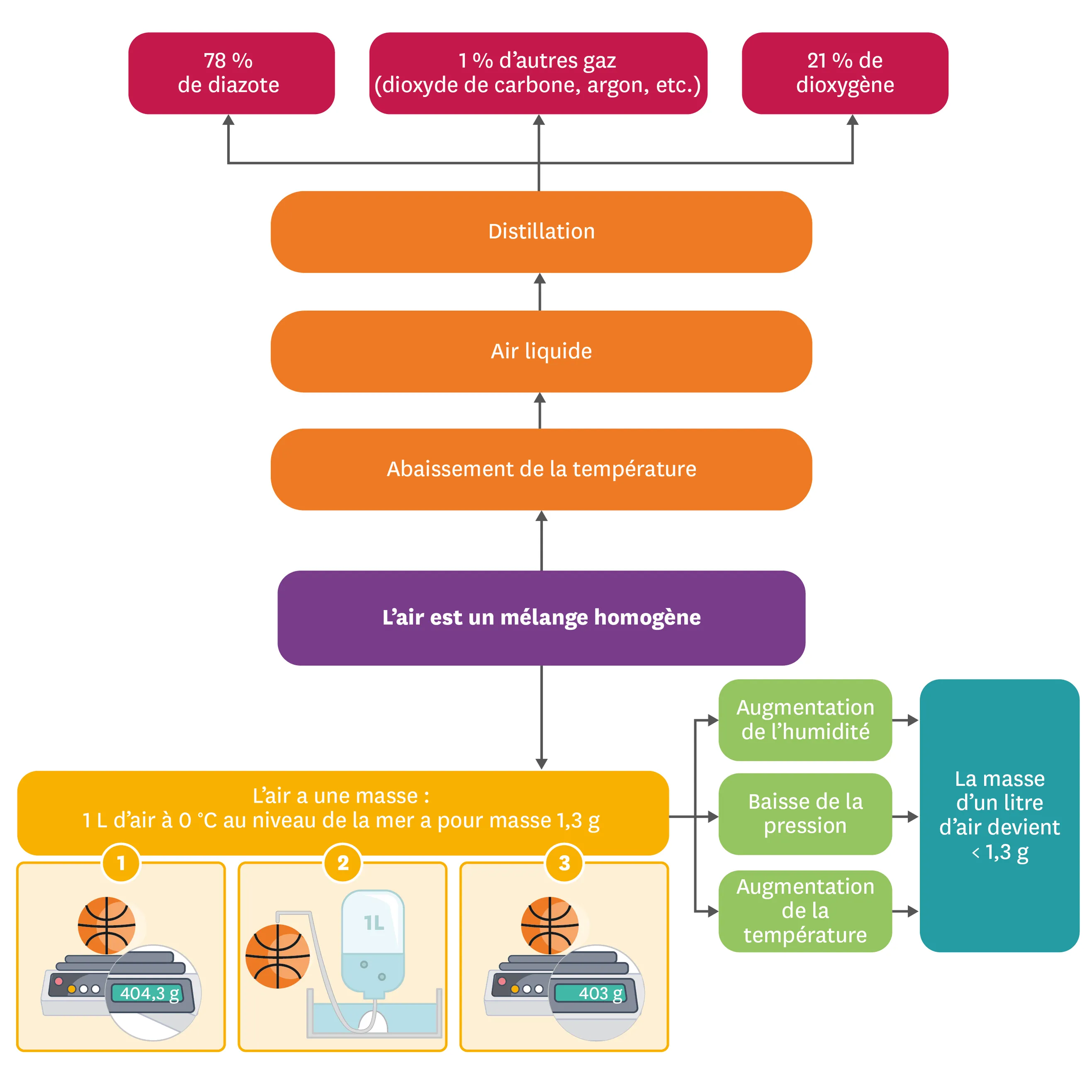
Je retiens par l'image

Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

