Chapitre 2
Activité 4 - Tâche complexe
De l'eau dans le gaz !
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétences :
Identifier le problème à résoudre.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Introduction
Louis a appris que la masse d'un litre d'air était de 1,3 g. Victor lui fait remarquer qu'il est important de savoir où a été prélevé ce litre d'air, car cela peut faire une différence.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Composition de l'air.
La composition chimique de l'air comprend pour l'essentiel du diazote, du dioxygène, des gaz rares, du dioxyde de carbone et de la vapeur d'eau qui intervient dans des proportions pouvant aller de 0,1 % à 5 %. Lorsque l'air contient beaucoup de vapeur d'eau, les proportions de ses autres composants sont moindres (on considère pour simplifier que certaines molécules de dioxygène ou de diazote sont remplacées par des molécules d'eau).
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
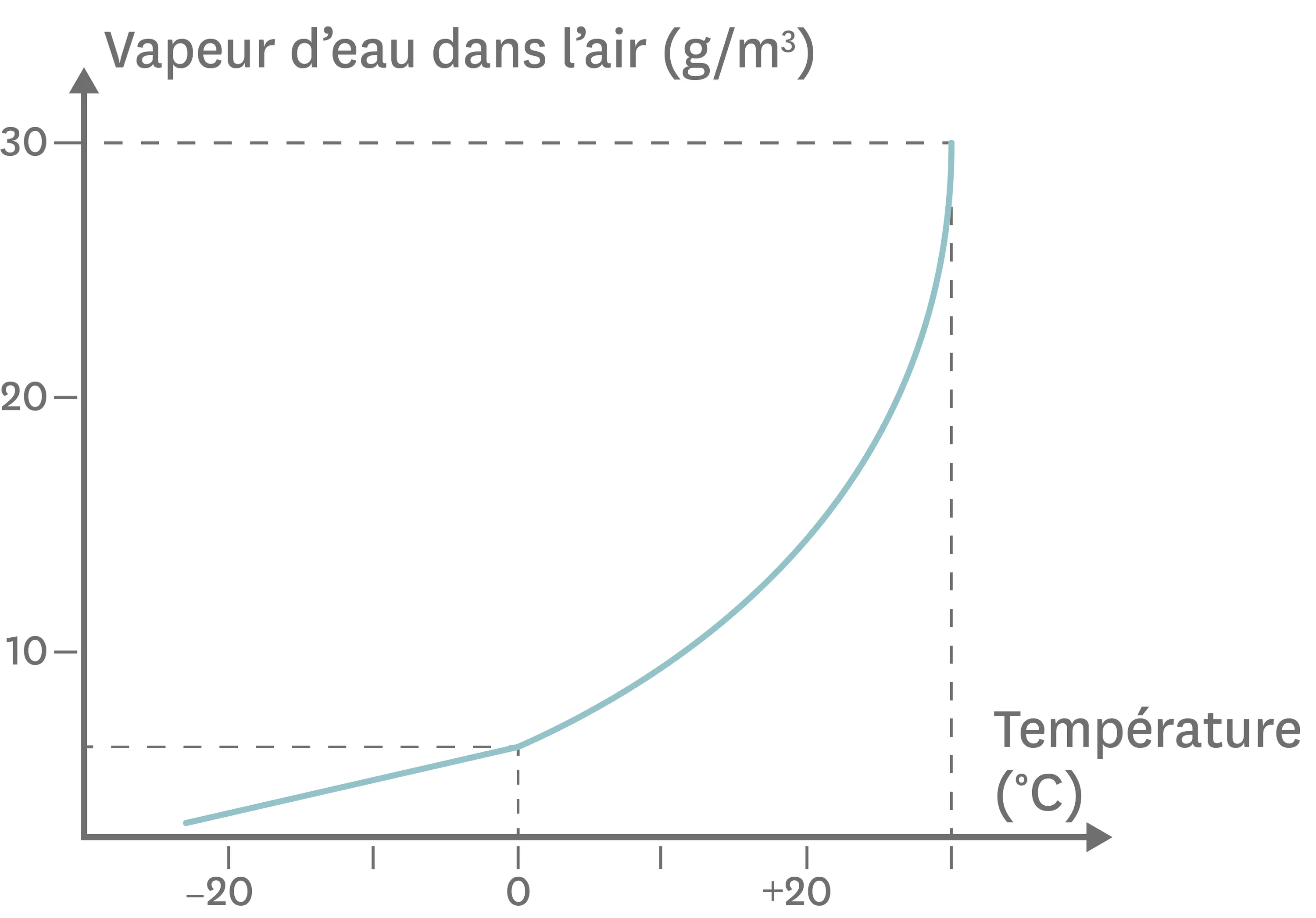
Doc. 2Masse maximale de vapeur d'eau par m3 d'air en fonction de la température de l'air.

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 3Masse des molécules constituant l'air.
| Masse d'une molécule de diazote | 4,6 x 10-23 g |
| Masse d'une molécule de dioxygène | 5,3 x 10-23 g |
| Masse d'une molécule d'eau | 3,0 x 10-23 g |
| Masse d'une molécule de dioxyde de carbone | 7,3 x 10-23 g |
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 4Les climats.
Le mot « climat » renvoie à l'ensemble des phénomènes naturels atmosphériques en un lieu donné. Pour définir un climat, il faut procéder à l'analyse d'une série de mesures de grandeurs telles que la température et l'humidité de l'air du lieu concerné.
Par exemple, le climat équatorial est chaud et humide toute l'année. Quant au climat polaire, il est très froid avec des précipitations faibles, le plus souvent sous forme de neige.
Par exemple, le climat équatorial est chaud et humide toute l'année. Quant au climat polaire, il est très froid avec des précipitations faibles, le plus souvent sous forme de neige.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ta mission
La masse d'un litre d'air est égale à 1,3 g dans les conditions normales de température et de pression. Est-ce vrai quel que soit l'endroit où la mesure a été faite ? Tu répondras en t'appuyant sur des informations et des valeurs chiffrées issues des documents.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- Les conditions normales de température et de pression : conditions d'expérimentation et de mesures qui permettent de comparer des résultats T = O °C et P = 1 013 hPa.
- Une grandeur : information qui peut être mesurée, s'exprime à l'aide d'un nombre et d'une unité.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- J'ai expliqué le lien entre la masse de l'air et les proportions de ses composants.
- J'ai identifié des circonstances capables de faire varier la composition de l'air.
- J'ai utilisé des valeurs chiffrées pour illustrer mes explications.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

