Chapitre 5
Activité 3 - Activité documentaire
La compressibilité d'un gaz
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétence : Interpréter des résultats.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Problématique de l'activité


Pour pouvoir nager avec les dauphins, un plongeur emporte sur son dos une bouteille contenant une importante quantité d'air, comprimée dans un petit volume. Les parois métalliques de la bouteille résistent à la pression élevée de son contenu.
Le modèle particulaire explique-t-il que les gaz soient compressibles ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1La pression modélisée.

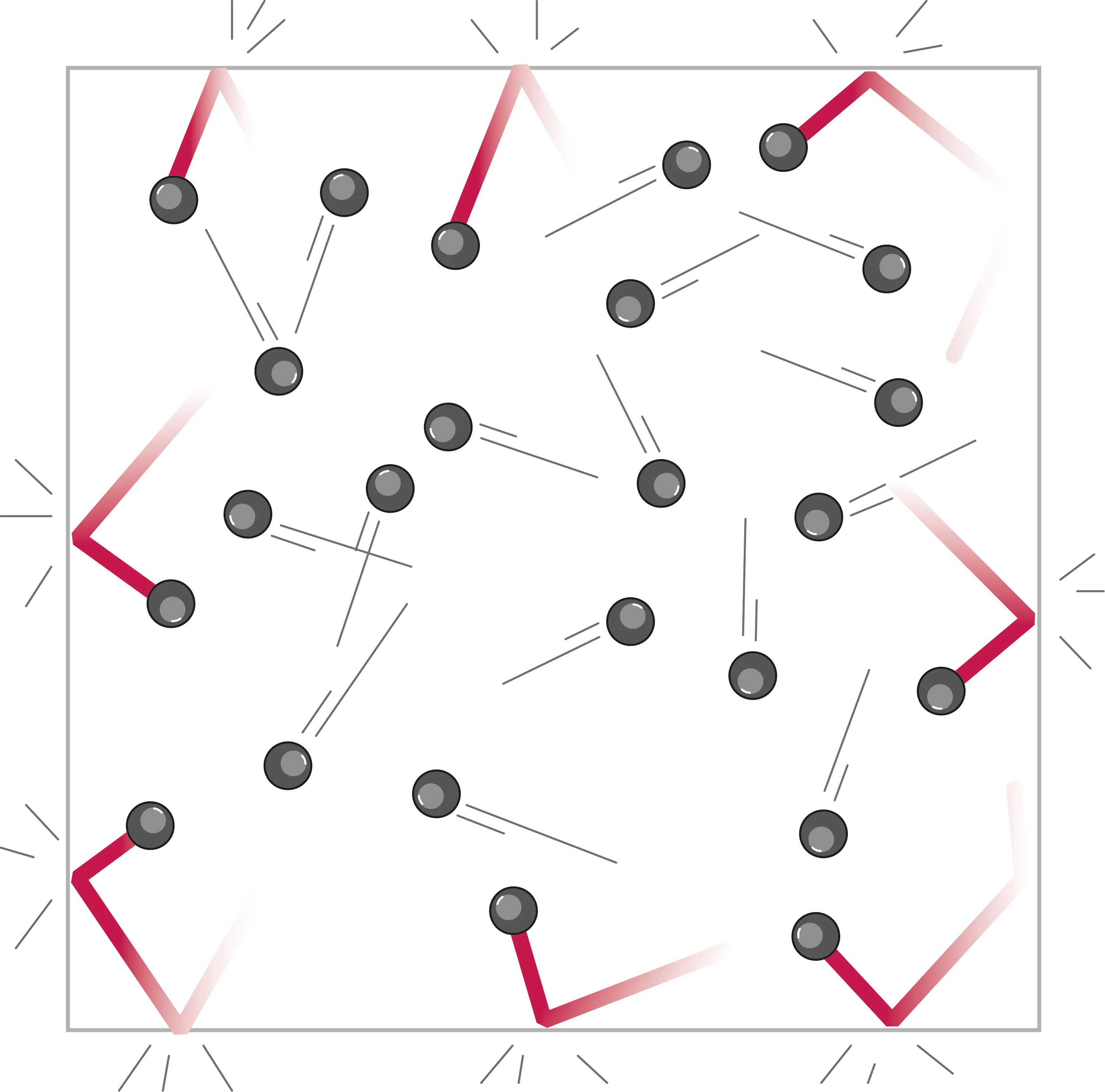
L'état gazeux est modélisé par le mouvement rapide et la dispersion des particules dans le vide. Dans ce modèle, la pression du gaz est le résultat de l'ensemble des collisions des particules sur la paroi.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
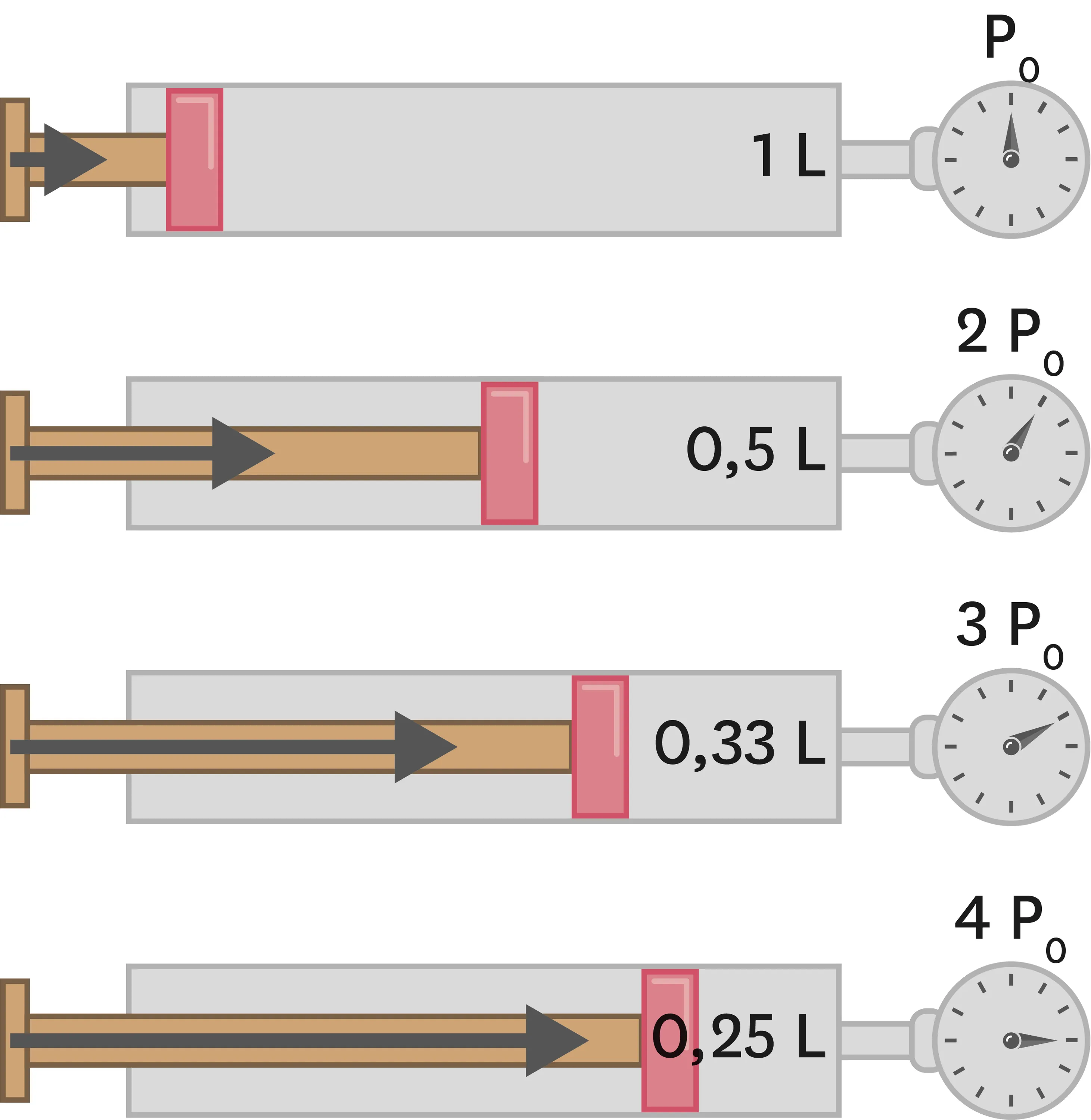
Doc. 2Évolution de la pression P de l'air quand on le comprime.

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Le vide : absence de toute matière dans un espace.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
Exploration et analyse des documents
1. Comment le modèle particulaire décrit-il l'état gazeux ?2. À quoi est due la pression d'un gaz sur les parois du récipient qui le contient ?
3. Comment varie la pression en fonction du volume du gaz ?
4. Schématise une seringue contenant 10 molécules dans la première position du piston.
5. Reprends ce schéma avec un piston placé dans la deuxième position.
Synthèse
6. Explique l'augmentation de la pression d'un gaz dont on diminue le volume, en utilisant le modèle particulaire et l'évolution du nombre de collisions au cours de cette opération.Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- J'ai modélisé des situations expérimentales en utilisant la notion de molécule.
- J'ai interprété la variation de la pression d'un gaz en utilisant le modèle particulaire de la matière.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

