Thème 1 - Organisation et transformations de la matière
Brevet
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ressources numériques
- concernant les transformations chimiques.
- De même, pour pouvoir
- Une simulation du site concernant la masse volumique.
- Pour et retrouver leur nom à partir des atomes qui les composent.
- De même, pour pouvoir observer de la matière à l'échelle microscopique selon les différents états.
- Pour le pH de différentes solutions.
- Pour apprendre à chimiques.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Sujet Brevet 1 : guidé15 min Développement
durable
Les dépôts sauvages
15 min
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétences
✔ Distinguer atomes, molécules et ions.✔ Connaître la structure d'un atome et ses constituants.
✔ Mettre en œuvre des tests caractéristiques.
✔ Déterminer une masse volumique.
✔ Exploiter des mesures pour différencier des espèces chimiques, des corps purs ou des mélanges.
Introduction
De nombreuses décharges sauvages, en dehors des
déchetteries conventionnelles, sont recensées chaque jour.
La pollution qui en résulte ne peut alors pas être traitée et a
des conséquences néfastes sur l'environnement.
On retrouve parfois des barils dans ces dépôts. On se
propose d'étudier le liquide issu de l'un de ces barils.Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Étude de l'échantillon
On dépose une goutte de l'échantillon
sur du sulfate de cuivre anhydre \mathrm{CuSO}_4.
Ce solide devient bleu.
En ajoutant quelques gouttes d'hydroxyde de sodium \left(\mathrm{Na}^{+} ; \mathrm{HO}^{-}\right) à l'échantillon, un précipité de couleur rouille se forme.
Ce solide devient bleu.
En ajoutant quelques gouttes d'hydroxyde de sodium \left(\mathrm{Na}^{+} ; \mathrm{HO}^{-}\right) à l'échantillon, un précipité de couleur rouille se forme.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 2Masses volumiques
| Matériau | Aluminium | Acier | Plomb |
| Masse volumique \left(\mathrm{kg} / \mathrm{m}^3\right) | 2 700 | 7 800 | 11 350 |
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
1. Un noyau de cuivre est représenté par la notation { }_{29}^{63} \mathrm{Cu}. Déterminer
le nombre de protons, de neutrons et d'électrons que contient un ion
cuivre \mathrm{Cu}^{2+}. Justifier la réponse.
Aide
1. Dans le symbole d'un
noyau \mathrm{_Z^A X}, \mathrm{A} donne le
nombre de nucléons
(protons + neutrons) et \mathrm{Z} le
nombre de protons. L'ion
cuivre \mathrm{Cu}^{2+} est un ion positif
(cation) : il se forme quand
l'atome de cuivre perd deux
électrons.
2. À l'aide de la fiche 5, préciser le nom des espèces chimiques
identifiées dans l'échantillon étudié dans le Doc. 1.
Aide
2. Comparer les résultats
obtenus dans le Doc. 1. aux
tests d'identification fournis.
3. Un échantillon du baril est prélevé. Sa masse est m = \text{46,8 } g pour
un volume \text{V = 6,0 mL}. Déterminer la nature du matériau constituant
le baril.
Aide
3. Le Doc. 2 indique que les
matériaux se différencient
par leur masse volumique. Il
faut donc calculer la masse
volumique \rho de l'échantillon
et comparer le résultat aux
données du Doc. 2.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Sujet Brevet 2 : non guidé15 minEnjeux énergétiques
La voiture à dihydrogène
15 min
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétences
✔ Distinguer atomes, molécules et ions.✔ Interpréter une formule chimique en termes atomiques.
✔ Connaître la structure d'un atome et ses constituants.
✔ Distinguer les types de transformations.
✔ Interpréter les transformations chimiques comme des redistributions d'atomes sans modification de la masse totale.
Introduction
Avec la fin programmée pour 2035 de la vente de véhicules thermiques neufs basés sur la combustion de carburants, les constructeurs se tournent vers de nouvelles technologies, comme les voitures à dihydrogène, souvent appelées voitures à hydrogène dans le langage courant.Le dihydrogène \mathrm{H_2} nécessaire au fonctionnement de ces véhicules peut être produit à partir de matières fossiles. On parle alors de dihydrogène « gris ». On peut aussi le produire par électrolyse de l'eau \mathrm{H_2O} en utilisant de l'énergie électrique provenant de sources renouvelables.
On parle alors de dihydrogène « vert ». En roulant, ce type de voiture n'émet pas de dioxyde de carbone \mathrm{CO_2}.


Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Quelques atomes d'hydrogène
Ce document présente quelques informations sur différents
atomes d'hydrogène.
Symbole : \mathrm{^1_1H}
Numéro atomique : 1
Nombre d'électrons : 1
Nombre de nucléons : 1
Symbole : \mathrm{^2_1H}
Numéro atomique : 1
Nombre d'électrons : 1
Nombre de nucléons : 2
Symbole : \mathrm{^3_1H}
Numéro atomique : 1
Nombre d'électrons : 1
Nombre de nucléons : 3
Hydrogène 1
Numéro atomique : 1
Nombre d'électrons : 1
Nombre de nucléons : 1
Hydrogène 2 (deutérium)
Numéro atomique : 1
Nombre d'électrons : 1
Nombre de nucléons : 2
Hydrogène 3 (tritium)
Numéro atomique : 1
Nombre d'électrons : 1
Nombre de nucléons : 3
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 2Électrolyse de l'eau
L'équation de la réaction de l'électrolyse
de l'eau est la suivante.
2 \mathrm{H}_2 \mathrm{O} \rightarrow 2 \mathrm{H}_2+\mathrm{O}_2
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
1. À l'aide des informations du Doc. 1, préciser le nombre de protons dans chacun des atomes
d'hydrogène \mathrm{H} présentés ainsi que leurs nombres de neutrons et d'électrons. Justifier la réponse.
2. À l'aide des informations fournies, donner la composition en atomes d'une molécule d'eau.
3. Indiquer si l'électrolyse de l'eau est une transformation physique ou chimique. Justifier la réponse.
4. Pour faire le plein d'une voiture à hydrogène, il est nécessaire d'électrolyser 2 \times 10^{24} molécules d'eau \mathrm{H}_2 \mathrm{O}.
En déduire le nombre de molécules de dihydrogène \mathrm{H_2}
et de dioxygène \mathrm{O_2} formées. Justifier la réponse.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Sujet Brevet 3 : guidé15 minChangement
climatique
Les incendies de forêts
15 min
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétences
✔ Interpréter une formule chimique en termes atomiques.✔ Évoquer quelques gaz de l'atmosphère et les gaz à effet de serre.
✔ Utiliser une équation de réaction chimique pour décrire une transformation.
✔ Connaître quelques propriétés des transformations chimiques.
✔ Identifier les gaz à effet de serre produits lors de transformations chimiques
Introduction
L'été 2022 a été marqué par une sécheresse inédite en
France, causant de nombreux incendies de forêts.
Ce phénomène risque de se reproduire de plus en plus
fréquemment à cause du changement climatique.

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Combustion du bois
Le bois est composé en partie de cellulose. La cellulose est un polymère,
c'est-à-dire une chaîne de molécules de glucose \mathrm{C}_6 \mathrm{H}_{12} \mathrm{O}_6. Quand il brûle,
le glucose réagit avec le dioxygène \mathrm{O_2}
présent dans l'air pour former de
l'eau \mathrm{H_2O} et du dioxyde de carbone \mathrm{CO_2}.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
1. À l'aide du Doc. 1, préciser la composition atomique d'une molécule de glucose.
Aide
1. La formule du glucose
donnée dans le Doc. 1
indique les atomes qui la
constituent et le nombre
de chacun d'eux.
2. À l'aide du Doc. 1, préciser les réactifs (combustible et comburant) et
les produits formés dans la réaction de combustion du glucose.
Aide
2. Le combustible et
le comburant sont les
réactifs d'une réaction
de combustion. Les
produits sont les espèces
chimiques formées par
une réaction.
3. Parmi les propositions suivantes, indiquer celle qui correspond à
l'équation de réaction de combustion de la cellulose. Justifier la réponse.
Aide
3. Une équation de
réaction traduit la
conservation des
atomes au cours d'une
transformation. Elle doit
être équilibrée.
4. Expliquer en quoi les incendies de forêts participent également au
changement climatique.
Aide
4. La vapeur d'eau \mathrm{H_2O}
et le dioxyde de carbone \mathrm{CO_2}
sont des gaz à effet de serre.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Sujet Brevet 4 : non guidé 15 minChangement
climatique
L'acidification des océans
15 min
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétences
✔ Interpréter une formule chimique en termes atomiques.✔ Identifier expérimentalement le caractère acide ou basique d'une solution.
✔ Associer le caractère acide ou basique à la présence d'ions \mathrm{H}^{+} et \mathrm{HO^-}.
Introduction
Les océans absorbent une partie du dioxyde de carbone \mathrm{CO_2} présent dans l'atmosphère, contribuant ainsi
à ralentir le processus de réchauffement climatique. En se dissolvant dans l'eau, le dioxyde de carbone \mathrm{CO_2}
entraîne une modification du pH des océans. L'acidification des océans diminue alors la quantité d'ions hydrogénocarbonate \mathrm{HCO_3^-} nécessaires à la formation du squelette des coraux et autres structures calcaires.Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
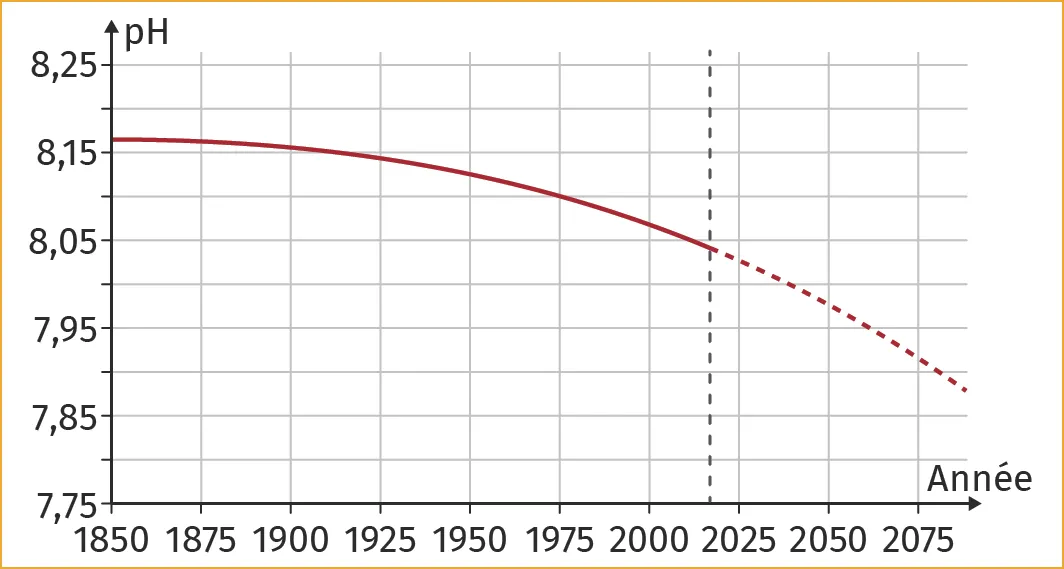
Doc. 1Évolution du pH des océans
Le graphique ci-contre montre l'évolution du pH des océans au cours du temps et les prévisions pour les décennies à venir.

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
1. À l'aide des informations fournies, préciser la composition en atomes d'une molécule de dioxyde de carbone.
2. Proposer un protocole pour mesurer le pH d'un échantillon d'eau de mer.
3. Compléter le schéma ci-dessous en plaçant les propositions suivantes au bon endroit : acide, basique,
neutre, ions hydroxyde \mathrm{HO^-} majoritaires, ions hydrogène \mathrm{H^+} majoritaires.
4. À l'aide du Doc. 1, indiquer comment évolue le pH des océans au cours du temps.
5. Expliquer l'expression « acidification des océans ».
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

