Chapitre 3
Activité 4 - Tâche complexe
Une protection bidon ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétences : Mettre en oeuvre un raisonnement logique simple pour résoudre un problème.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Introduction


Le zinc est un métal utilisé pour prolonger la durée d'utilisation des objets en fer ou en acier. Lors d'un procédé appelé galvanisation, une mince couche de zinc est déposée à la surface du fer et retarde sa dégradation chimique. Utilisés en grande quantité dans les industries, les produits ménagers peuvent être stockés dans des bidons en acier galvanisé.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Action de l'acide sulfurique sur le zinc.


On observe un dégagement gazeux. Ce gaz donne une petite détonation à l'approche d'une flamme.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 2Tests d'identification réalisés sur la solution obtenue à la fin de la réaction (voir significations au chapitre précédent).


Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 3Espèces chimiques et formules.
| Ion sulfate | SO42- |
| Atome de zinc | Zn |
| Ion zinc | Zn2+ |
| Dihydrogène | H2 |
| Ion hydrogène | H+ |
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
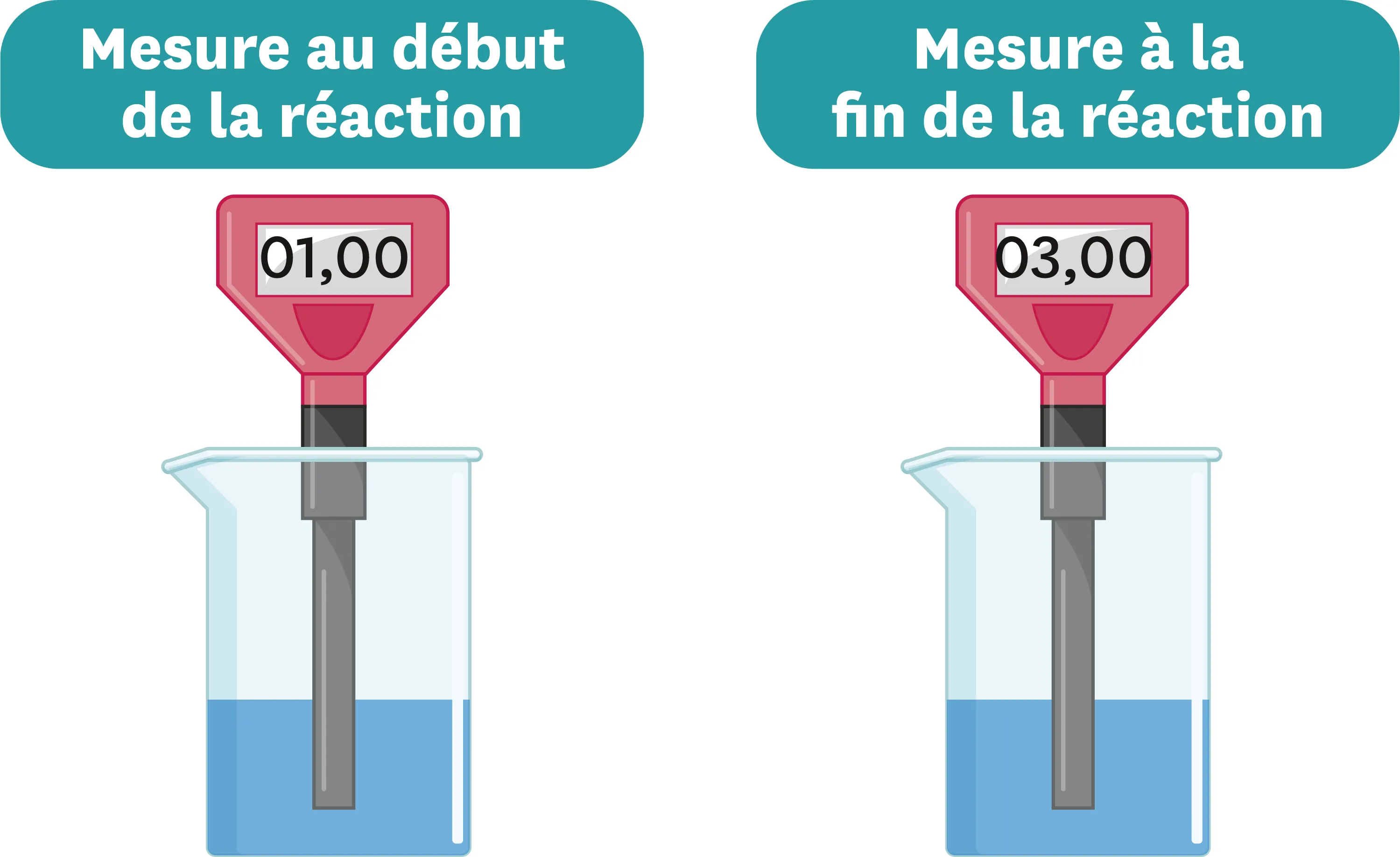
Doc. 4Évolution du pH de la solution obtenue au cours de la réaction.

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ta mission
Pourquoi la couche de zinc déposée à la surface du bidon ne fait-elle que retarder la corrosion ? À partir des documents, détermine si ce métal est concerné par la corrosion et écris l'équation de réaction qui correspond si c'est le cas.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- J'ai associé les différents tests présentés aux espèces chimiques correspondantes.
- J'ai identifié les espèces chimiques dont les quantités ont changé.
- J'ai expliqué pourquoi le zinc ne fait que retarder la corrosion du fer et de l'acier.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

