Exclu. numérique 2023
Chapitre 7
Bilan
Modélisation des transformations physiques
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Exclu. numérique 2023
Retrouvez sur les transformations endothermiques et exothermiques.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
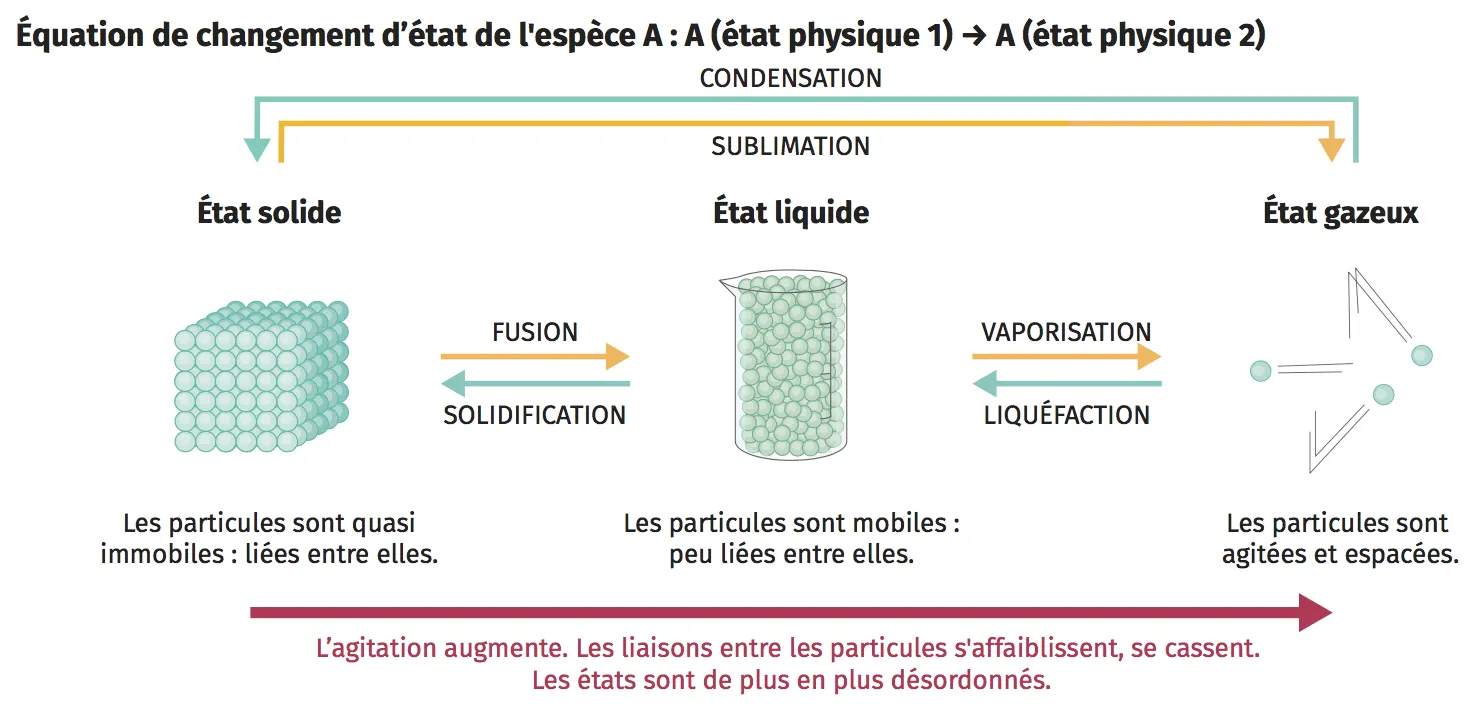
Modélisation des transformations physiques

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Les échanges d'énergie

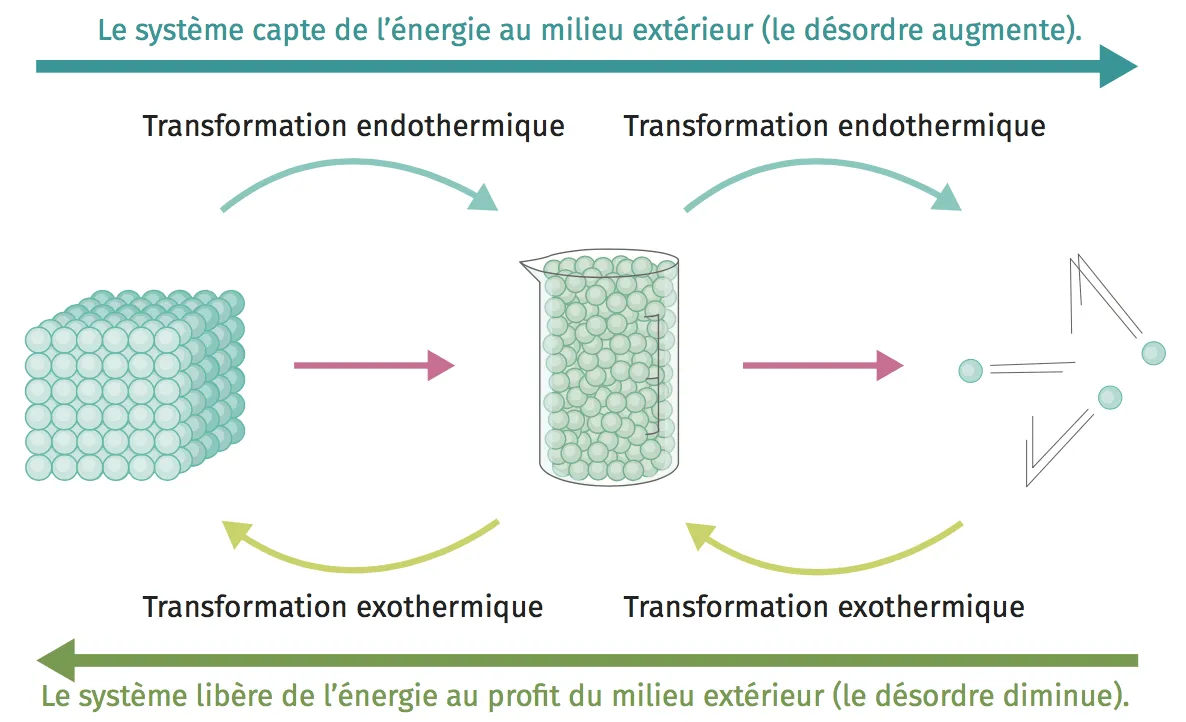
Énergie reçue ou libérée par transfert thermique lors d'un changement d'état : Q = m \cdot L,
avec Q quantité d'énergie transférée en Joule (J), m masse du corps en kilogramme (kg) et L énergie massique de changement d'état en J·kg-1. Elle est aussi appelée chaleur latente de changement d'état ou enthalpie de changement d'état.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Les limites de la modélisation
Le modèle particulaire représente de façon simplifiée la réalité étudiée. Les molécules, atomes ou ions sont représentés par des sphères de couleur supposées rigides, insécables et indéformables.
Ce modèle permet :
- de représenter les trois principaux états physiques de la matière et de comprendre leurs propriétés ;
- de distinguer les notions de fusion et dissolution ;
- d'interpréter les effets d'un chauffage ou d'un refroidissement au niveau macroscopique.
Mais il ne permet pas :
- de comprendre que les énergies massiques de changement d'état dépendent de la pression et de la température ;
- de comprendre certains phénomènes, comme la surfusion de la glace.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Vidéo bilan : Les changements d'état physique de la matière


00:00 / --:--
