Chapitre 7
Fiche de révision
Exclusivité numérique
Modélisation des transformations physiques
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Plan
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
1Modélisation des transformations physiques
AChangement d'état physique
- La matière qui nous entoure peut se trouver sous trois états physiques différents : solide, liquide, gaz.
- Lorsque la matière change d'état physique, ses propriétés et l'arrangement spatial de ses molécules sont modifiés.

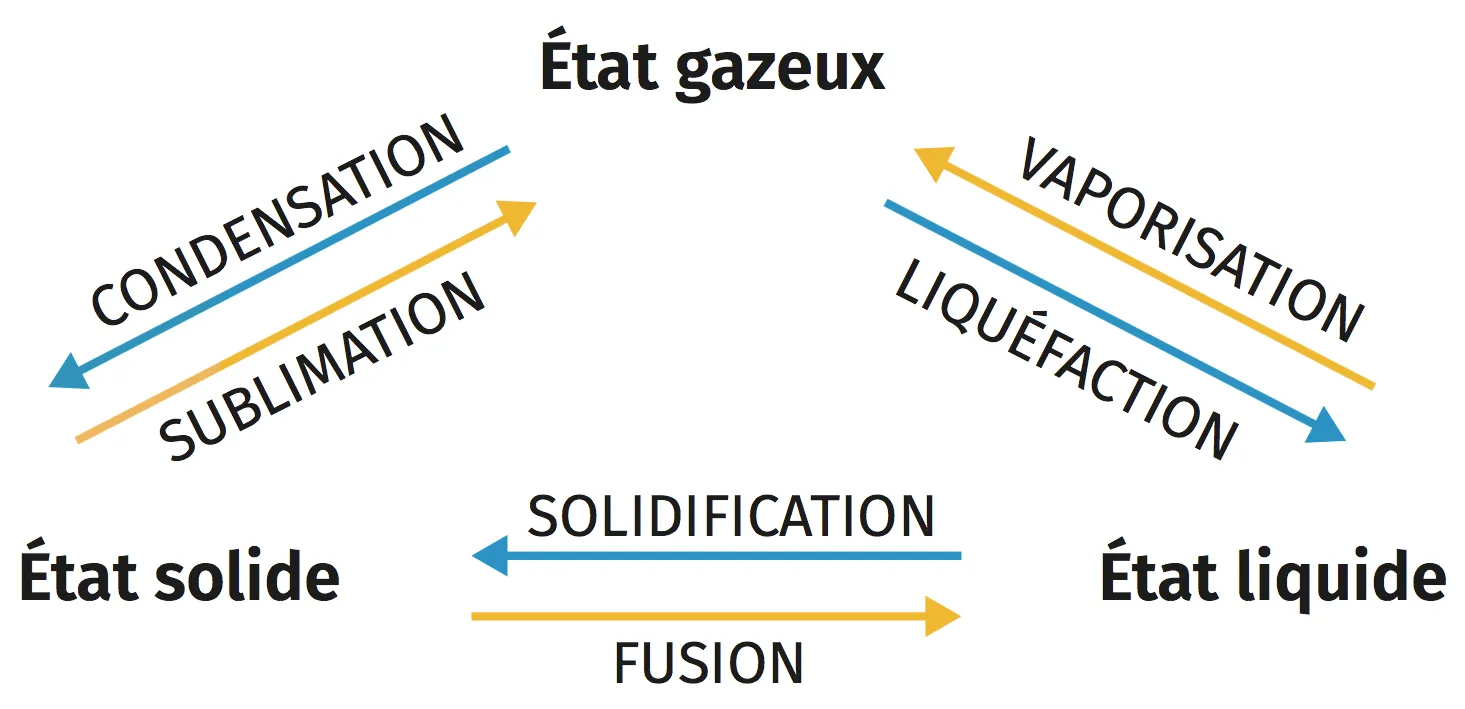
BÉcriture symbolique d'un changement d'état
- Pour modéliser le changement d'état physique de l'espèce chimique A, on écrit :
\text{ A (état physique 1)} \rightarrow \text{ A (état physique 2)}
CModélisation microscopique d'un changement d'état
- Un gaz : composé d'espèces chimiques libres, sans liaison entre elles, qui se choquent sans cesse.
Dans un gaz, les particules sont agitées et espacées.
- Un liquide : constitué d'espèces chimiques en mouvement, reliées entre elles par des liaisons faibles.
Dans un liquide, les particules sont mobiles et peu liées entre elles. - Un solide : formé d'espèces chimiques fortement liées les unes aux autres, ne disposant que de peu de liberté de mouvement. Dans un solide, les particules sont quasi immobiles, et liées entre elles.
- Un changement d'état entraîne une modification de l'agitation des espèces au niveau microscopique. Les liaisons entre les particules s'affaiblissent, se cassent ou se créent.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
2Les échanges d'énergie
ATransformations physiques endothermiques
et exothermiques
- Un corps chauffé capte de l'énergie au milieu extérieur :
la transformation est endothermique.
L'agitation des particules est plus grande, les liaisons entre les particules peuvent se rompre et le désordre augmente. Exemples : la fusion, la vaporisation ou la sublimation. - Lorsque le corps se refroidit, la transformation est exothermique.
L'agitation des particules diminue, elles peuvent créer de nouvelles liaisons et l'ordre se fait.
Exemples : la solidification, la condensation et la liquéfaction.
BÉnergie de changement d'état
- \Delta E représente l'énergie acquise ou perdue lors d'un changement d'état. Elle provient d'un transfert thermique Q avec un autre système, d'où Q = \Delta E.
- On en déduit : Q = m \cdot L
avec :
Q la quantité d'énergie transférée en Joule (J) ;
m la masse du corps en kilogramme (kg) ;
L l'énergie massique de changement d'état en J·kg-1. - L est aussi appelée chaleur latente de changement d'état ou enthalpie de changement d'état.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Les limites de la modélisation
Le modèle particulaire est une représentation simplifiée de la réalité.
Les molécules, atomes ou ions sont représentés par des sphères de couleur supposées rigides, insécables et indéformables.
Les molécules, atomes ou ions sont représentés par des sphères de couleur supposées rigides, insécables et indéformables.
-
Ce modèle permet :
- de représenter les trois principaux états physiques de la matière et de comprendre leurs propriétés ;
- de distinguer les notions de fusion et dissolution ;
- d'interpréter les effets d'un chauffage ou d'un refroidissement au niveau macroscopique.
-
Mais il ne permet pas de :
- de comprendre que les énergies massiques de changement d'état dépendent de la pression et de la température ;
- de comprendre certains phénomènes, comme la surfusion de la glace.