Chapitre 7
Activité 1 - Activité d'exploration
Du microscopique au macroscopique
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Problématique de l'activité
Une coupelle contenant une solution aqueuse de chlorure de sodium saturée
laisse apparaître après quelques jours de magnifiques cristaux cubiques !
Quelles propriétés des entités constituant le sel sont à l'origine de sa
structure ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Les cristaux ont-ils tous
la même structure ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1 L'interaction électrostatique
Deux corps ponctuels \text{A} et \text{B}, portant des charges
électriques respectives q_\text{A} et q_\text{B}, s'attirent ou se
repoussent mutuellement avec des forces d'égales
intensités, mais opposées vectoriellement.
L'attraction ou la répulsion qu'ils exercent l'un sur l'autre est :
La valeur de la force de Coulomb est donnée par la relation :
avec k la constante de Coulomb (k = 9\text{,}0 \times 10^{9} N·m2·C-2), F en newton (N), q_\text{A} et q_\text{B} en coulomb (C) et \text{d}
en m.
L'attraction ou la répulsion qu'ils exercent l'un sur l'autre est :
- proportionnelle à leurs charges q_\text{A} et q_\text{B} ;
- inversement proportionnelle au carré de la distance d qui les sépare.
La valeur de la force de Coulomb est donnée par la relation :
F=k \cdot \dfrac{|q_{\mathrm{A}} \cdot q_{\mathrm{B}}|}{\mathrm{d}^{2}}
avec k la constante de Coulomb (k = 9\text{,}0 \times 10^{9} N·m2·C-2), F en newton (N), q_\text{A} et q_\text{B} en coulomb (C) et \text{d}
en m.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Retrouvez pour visualiser la force électrique qui s'applique sur un capteur placé
à proximité d'une charge électrique positive ou négative.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
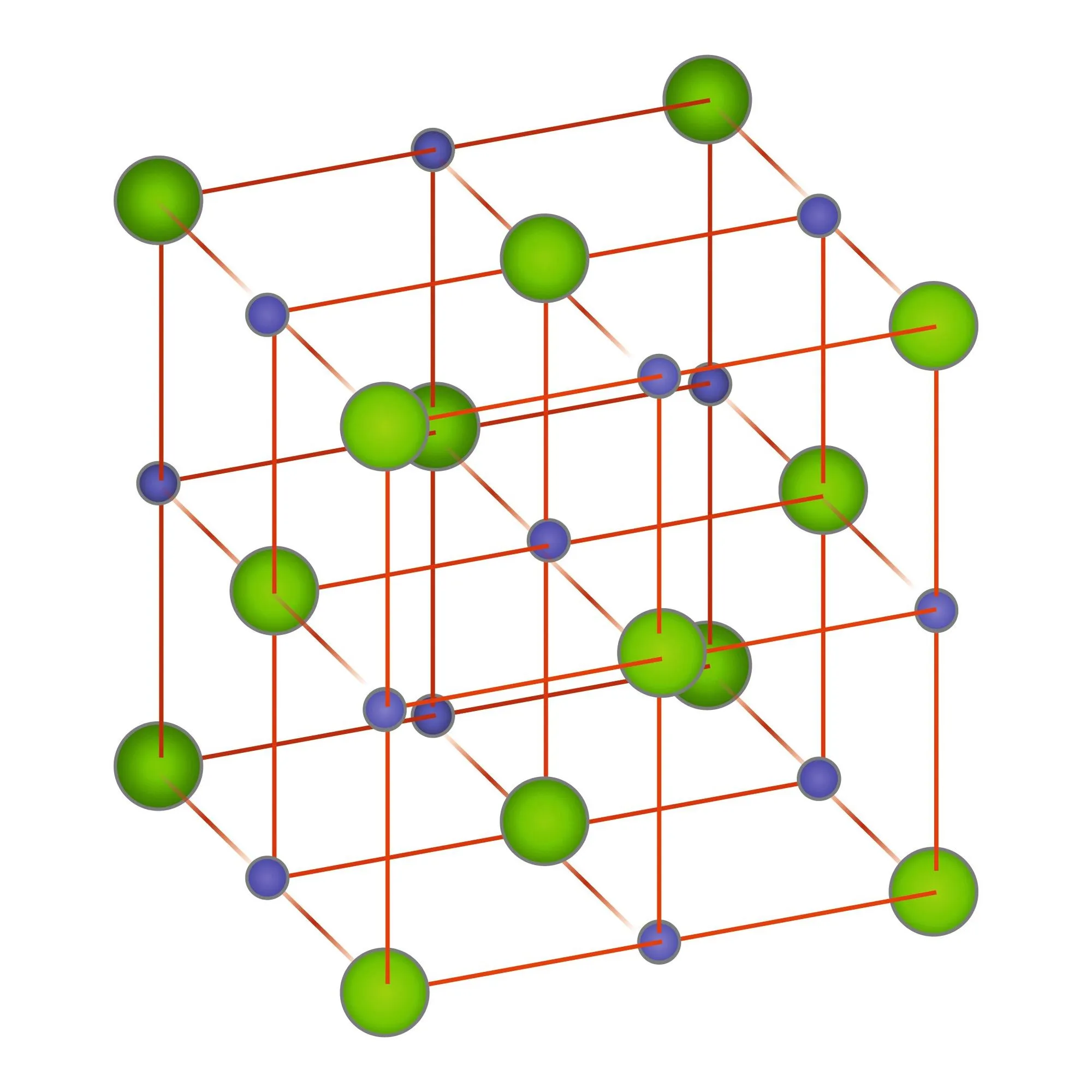
Doc. 2Organisation des ions dans le cristal
Dans le solide, les ions chlorure \text{Cl}^- et les ions sodium \text{Na}^+
sont organisés dans un empilement périodique et symétrique.
C'est un réseau cubique à faces centrées. Les ions chlorure
occupent les sommets d'un cube d'arête a, et le milieu de chacune
des faces. Les ions sodium occupent le centre du cube et
le centre de chacune des arêtes du cube. La distance entre un
cation et un anion voisin est égale à \dfrac a2 .
La distance entre deux
cations ou deux anions proches est égale à : a \dfrac{\sqrt{2}}{2}.
Retrouvez plus d'informations sur .
Retrouvez plus d'informations sur .
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 3 Le cristal de chlorure de sodium



Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
Compétence(s)
RAI/ANA : Faire le
lien entre les modèles
microscopiques et les
grandeurs macroscopiques
1. Doc. 1 Comment la valeur de la force de Coulomb évolue-t-elle si la distance entre deux charges ponctuelles est divisée par deux ?
2. Doc. 2 Quelle est la valeur de la charge électrique portée par un ion chlorure ? Et celle portée par un ion sodium ?
3. Calculer la valeur de la force qui s'exerce entre deux ions chlorure proches puis entre un ion sodium et un ion chlorure voisins. Les comparer. (Charge élémentaire : e = 1\text{,}6 \times 10^{-19} C).
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Synthèse de l'activité
Expliquer l'origine de la cohésion des solides ioniques.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

