Chapitre 8
Exercices
Pour s'entraîner
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
22Formation de plomb
✔ RAI/ANA : Utiliser et interpréter des documents
On réalise l'électrolyse d'une solution aqueuse de nitrate de plomb (\text{Pb}^{2+}(\text{aq}) \; ; \; 2\ \text{NO}_3^-(\text{aq})) dans un électrolyseur dont l'électrode de graphite est reliée à la borne positive du générateur et l'électrode de plomb à la borne négative. Un dépôt de plomb \text{Pb(s)} se forme sur l'électrode de graphite et un dégagement gazeux de dioxygène apparaît à l'autre électrode. L'intensité du courant est maintenue à 300 mA durant 1 h 30.
1. Écrire les demi-équations de réactions aux électrodes ainsi que l'équation de la réaction d'électrolyse.
2. Préciser si l'électrode de plomb joue le rôle d'anode ou de cathode.
3. Exprimer la quantité de matière de plomb formée en fonction de l'intensité du courant et de la durée de l'électrolyse.
4. Calculer la masse de la couche de plomb formée.
Données
- Couples d'oxydoréduction : \text{Pb}^{2+}\text{(aq)/Pb(s)} et \text{O}_2\text{(g)/H}_2\text{O(l)}
- Masse molaire du plomb : M(\text{Pb}) = 207{,}2 g·mol-1
- Constante de Faraday : F = 96\ 500 C·mol-1
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
23Réflexion en QCM
✔ APP : Extraire l'information utile
On dispose d'un mélange d'une solution de nitrate d'argent (\text{Ag}^+(\text{aq})\; ; \; \text{NO}_3^-(\text{aq})) de concentration \text{0,10} mol·L-1 et d'une solution concentrée à \text{0,50} mol·L-1 de sulfate de cuivre (\text{Cu}^{2+}(\text{aq}) \; ; \; \text{SO}_4^{2-}(\text{aq})), d'un fil d'argent, d'une lame de cuivre et d'un générateur de courant continu.
À l'aide de ce matériel, on réalise une électrolyse dont l'équation de réaction est :
2\ \text{Ag(s)} + \text{Cu}^{2+}(\text{aq}) \rightarrow 2\ \text{Ag}^+(\text{aq}) + \text{Cu(s)}
La constante d'équilibre de cette réaction est K = 4{,}7 \times 10^{-16}.
1. Le quotient de réaction initial de ce système pour l'équation donnée est :
2. Préciser quelle plaque est reliée au pôle positif du générateur et la nommer.
3. L'expression de la quantité de matière de \text{Cu(s)} déposée est :
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
24Constante de Faraday
✔ VAL : Identifier et évaluer les sources d'erreurs


L'électrozingage consiste à recouvrir des pièces en fer ou en acier par une couche de zinc déposée par électrolyse. Ainsi, la pièce de fer est protégée de la corrosion.
Au laboratoire, on pèse une plaque de zinc m_1 = 28{,}42 g, puis on réalise un montage d'électrolyse avec une solution de chlorure de zinc (\text{Zn}^{2+}(\text{aq})\; ; \; 2\; \text{Cl}^-(\text{aq})), une plaque de fer reliée au pôle négatif du générateur et la plaque de zinc à l'autre pôle. Un courant d'intensité \text{0,420} A circule dans le montage durant 50 min, puis la plaque de zinc est séchée et pesée : on obtient m_2 = 28{,}00 g.
Au laboratoire, on pèse une plaque de zinc m_1 = 28{,}42 g, puis on réalise un montage d'électrolyse avec une solution de chlorure de zinc (\text{Zn}^{2+}(\text{aq})\; ; \; 2\; \text{Cl}^-(\text{aq})), une plaque de fer reliée au pôle négatif du générateur et la plaque de zinc à l'autre pôle. Un courant d'intensité \text{0,420} A circule dans le montage durant 50 min, puis la plaque de zinc est séchée et pesée : on obtient m_2 = 28{,}00 g.
1. Écrire la demi-équation de la réaction électrochimique ayant lieu à l'électrode de zinc.
2. Préciser le rôle de la plaque de zinc.
3. Relier la variation de masse de l'électrode de zinc à la quantité de matière d'électrons n_\text{e}.
4. Exprimer la constante de Faraday F en fonction de I, \Delta t et la variation de masse de zinc.
5. En déduire une valeur de la constante de Faraday. Déterminer les sources possibles d'incertitude.
2. Préciser le rôle de la plaque de zinc.
3. Relier la variation de masse de l'électrode de zinc à la quantité de matière d'électrons n_\text{e}.
4. Exprimer la constante de Faraday F en fonction de I, \Delta t et la variation de masse de zinc.
5. En déduire une valeur de la constante de Faraday. Déterminer les sources possibles d'incertitude.
Détails du barème
TOTAL / 5 pts
0,5 pt
1. Utiliser les informations du texte.0,5 pt
2. Connaître la définition d'anode et de cathode.1,5 pt
3.Exprimer n(\text{Zn})_\text{perdu} et n_\text{e}, puis relier avec la variation de masse.
1,5 pt
4. Expression de F en utilisant les expressions de Q.1 pt
5. Effectuer l'application numérique et évaluer les sources d'erreurs.
Données
- Couple d'oxydoréduction : \text{Zn}^{2+}\text{(aq)/Zn(s)}
- Masse molaire du zinc : M(\text{Zn}) = 65{,}4 g·mol-1
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
25Préparation de l'eau de Javel
✔ COM : Rédiger correctement une résolution d'exercice
L'eau de Javel ou hypochlorite de sodium se prépare industriellement par réaction du dichlore \text{Cl}_2(\text{g}) avec la soude (\text{Na}^+(\text{aq}) \; ; \; \text{HO}^-(\text{aq})). Le dichlore est obtenu par électrolyse d'une solution de chlorure de sodium (\text{Na}^+(\text{aq})\; ; \; \text{Cl}^-(\text{aq})).
1. Écrire la demi-équation de réaction électrochimique associée à la formation de dichlore par électrolyse.
2. Nommer l'électrode où a lieu cette transformation.
Pour préparer l'eau de Javel de cette bouteille, il faut obtenir \text{15} L de dichlore gazeux à partir de la solution électrolysée en \text{2,0} h.
3. Montrer que l'intensité I du courant qui doit circuler dans l'électrolyseur est d'environ \text{17} A.
Données
- Constante de Faraday : F = 9{,}65 \times 10^4 C·mol‑1
- Volume molaire des gaz à 20 °C : V_\text{m} = 24{,}0 L·mol‑1
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
26Étamage d'une canette
✔ VAL : Analyser des résultats
L'étamage consiste à déposer une couche d'étain \text{Sn(s)} sur une surface métallique. Beaucoup de canettes de soda sont en fer-blanc, c'est-à-dire de l'acier recouvert d'étain à l'intérieur et à l'extérieur (sauf le couvercle qui est en aluminium). Ce recouvrement peut être réalisé par électrolyse avec une solution de sulfate d'étain acidifiée (\text{Sn}^{2+}(\text{aq}) \; ; \; \text{SO}_4^{2-}(\text{aq})) et un courant d'intensité \text{5,0} A. L'une des électrodes est en étain et l'autre est constituée de la plaque d'acier rectangulaire servant à réaliser le corps de la canette de longueur L = 21{,}0 cm et de largeur l = 11{,}0 cm. Pour que la couche d'étain ait une épaisseur de e = 30 μm, l'électrolyse doit durer un peu moins d'une heure.
1. Préciser le rôle de la plaque d'acier.
2. Calculer la surface d'acier à étamer.
3. Déterminer la masse d'étain à déposer sur la boîte.
4. Vérifier l'ordre de grandeur de la durée de l'électrolyse.
Données
- Couple d'oxydoréduction : \text{Sn}^{2+}\text{(aq)/Sn(s)}
- Masse volumique de l'étain : \rho_\text{Sn} = 7{,}3 g·cm-3
- Masse molaire de l'étain : M(\text{Sn}) = 118{,}7 g·mol-1
- Constante de Faraday : F = 96\ 500 C·mol-1
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
27
Copie d'élève à commenter
Proposer une justification pour chaque erreur relevée par le correcteur.
Le chromage est un traitement permettant d'obtenir des pièces très brillantes. Pour chromer une pièce métallique de 30 cm2, on réalise l'électrolyse d'une solution de chlorure de chrome (\text{Cr}^{3+}(\text{aq}) \; ; \; 3\; \text{Cl}^-(\text{aq})). On doit déposer une couche de chrome de 50 μm d'épaisseur.
1. Préciser le rôle joué par la pièce à chromer.
2. Calculer la masse de chrome à déposer sur la pièce.
3. En déduire la quantité de matière de chrome déposée sur la pièce métallique.
4. L'électrolyse dure 8,0 h, en déduire l'intensité du courant fourni.
Le chromage est un traitement permettant d'obtenir des pièces très brillantes. Pour chromer une pièce métallique de 30 cm2, on réalise l'électrolyse d'une solution de chlorure de chrome (\text{Cr}^{3+}(\text{aq}) \; ; \; 3\; \text{Cl}^-(\text{aq})). On doit déposer une couche de chrome de 50 μm d'épaisseur.
1. Préciser le rôle joué par la pièce à chromer.
2. Calculer la masse de chrome à déposer sur la pièce.
3. En déduire la quantité de matière de chrome déposée sur la pièce métallique.
4. L'électrolyse dure 8,0 h, en déduire l'intensité du courant fourni.
Données
- Couple d'oxydoréduction : \text{Cr}^{3+}\text{(aq)/Cr(s)}
- Masse molaire du chrome : M(\text{Cr}) = 52{,}0 g·mol-1
- Masse volumique du chrome : \rho(\text{Cr}) = 7{,}19 g·cm-3
- Constante de Faraday : F = 9{,}65 \times 10^4 C·mol-1
1. Les ions \text{Cr}^{3+}(\text{aq}) doivent s'oxyder en \text{Cr(s)}, donc c'est l'anode.
2. Le volume de chrome à déposer est :
AN : V = 30 \times 50 \times 10^{-4} = 0,15cm
AN : m(\text{Cr}) = 7{,}19 \times 0{,}15 = 1{,}1 g
3.
AN : n(\text{Cr}) = \dfrac{1{,}1}{52{,}0} = \xcancel{2{,}12} \times 10^{-2} mol
4. La demi-équation est :
On a donc \xcancel{n_\text{Cr} = 3\ n_\text{e}} soit :
AN : I = \dfrac{2{,}1 \times 10^{-2} \times 9{,}65 \times 10^4}{3 \times 8{,}0 \times 3\ 600} = \xcancel{0{,}023} A
2. Le volume de chrome à déposer est :
-
V = S \cdot e
AN : V = 30 \times 50 \times 10^{-4} = 0,15
-
m(\text{Cr}) = \rho \cdot V
AN : m(\text{Cr}) = 7{,}19 \times 0{,}15 = 1{,}1 g
3.
-
n(\text{Cr}) = \dfrac{m(\text{Cr})}{M(\text{Cr})}
AN : n(\text{Cr}) = \dfrac{1{,}1}{52{,}0} = \xcancel{2{,}12} \times 10^{-2} mol
4. La demi-équation est :
\text{Cr}^{3+}(\text{aq}) + 3\ \text{e}^- \rightarrow \text{Cr(s)}
On a donc \xcancel{n_\text{Cr} = 3\ n_\text{e}} soit :
-
I = \dfrac{Q}{\Delta t}
I = \dfrac{n_\text{e} \cdot F}{\Delta t}
\xcancel{I = \dfrac{n_\text{Cr} \cdot F}{3\ \Delta t}}
AN : I = \dfrac{2{,}1 \times 10^{-2} \times 9{,}65 \times 10^4}{3 \times 8{,}0 \times 3\ 600} = \xcancel{0{,}023} A
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
28Stockage de l'énergie solaire
✔ RAI/MOD : Utiliser avec rigueur le modèle de l'énergie
Doc. 1
Projet MYRTE


Près d'Ajaccio, une centrale électrique très particulière a vu le jour en 2012. La plateforme MYRTE produit et stocke de l'énergie à partir du rayonnement solaire. 3 000 m2 de panneaux photovoltaïques produisent du courant électrique alimentant des habitations, mais ce courant sert aussi à réaliser l'électrolyse de l'eau pour produire du dihydrogène et du dioxygène lors des moments de faible consommation d'énergie. Ces deux gaz sont ensuite utilisés pour faire fonctionner une pile à hydrogène pour produire du courant électrique au moment des pics de consommation. Ce procédé atteint 40 % de rendement global en électricité et cette centrale produit l'équivalent de la consommation d'énergie de 200 foyers. L'électrolyseur et la pile dégagent de l'énergie thermique récupérée pour produire de l'eau chaude et du chauffage sur le site. Ainsi, le rendement du système est de 70 %.
Doc. 2
Électrolyse de l'eau
Sous l'action d'un courant continu et en présence d'électrodes en platine, l'eau peut être électrolysée. Ainsi, du \text{H}_2(\text{g}) et du \text{O}_2(\text{g}) sont produits. Dans des conditions classiques, \text{10,0} m3 de dihydrogène peuvent être produits par heure à la pression atmosphérique. L'intensité du courant électrique nécessaire est de l'ordre de \text{10} kA.
1. Réaliser un diagramme des conversions d'énergie intervenant dans cette centrale.
2. Écrire l'équation de la réaction d'électrolyse de l'eau et les demi‑équations des réactions aux électrodes.
Cliquez pour accéder à une zone de dessin
2. Écrire l'équation de la réaction d'électrolyse de l'eau et les demi‑équations des réactions aux électrodes.
3. Déterminer la valeur de l'intensité du courant utilisé pour l'électrolyse.
Données
- Couples d'oxydoréduction : \text{H}^+\text{(aq)/H}_2(\text{g}) et \text{H}_2\text{O(l)/O}_2(\text{g})
- Constante de Faraday : F = 9{,}65 \times 10^4 C·mol‑1
- Volume molaire des gaz à 20 °C : V_\text{m} = 24 L·mol‑1
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
29Accumulateur au plomb
✔ RAI/ANA : Utiliser et interpréter des documents
La batterie de démarrage d'une automobile est constituée par l'association, en série, de plusieurs éléments d'accumulateurs au plomb. C'est Gaston Planté qui mit au point la première batterie rechargeable en 1859.
Un élément d'accumulateur comprend deux électrodes : l'une est en plomb métallique \text{Pb(s)}, l'autre est recouverte de dioxyde de plomb \text{PbO}_2(\text{s}). Elles sont immergées dans une solution aqueuse d'acide sulfurique (2\; \text{H}^+(\text{aq}) \; ; \; \text{SO}_4^{2-}(\text{aq})).
Au démarrage d'une voiture, la transformation ayant lieu dans la batterie est :
Pour recharger complètement cette batterie, il faut \text{6} h avec un courant d'intensité égale à \text{7,8} A.
Un élément d'accumulateur comprend deux électrodes : l'une est en plomb métallique \text{Pb(s)}, l'autre est recouverte de dioxyde de plomb \text{PbO}_2(\text{s}). Elles sont immergées dans une solution aqueuse d'acide sulfurique (2\; \text{H}^+(\text{aq}) \; ; \; \text{SO}_4^{2-}(\text{aq})).
Au démarrage d'une voiture, la transformation ayant lieu dans la batterie est :
\text{Pb(s)} + \text{PbO}_2(\text{s}) + 4\ \text{H}^+(\text{aq}) \rightarrow 2\ \text{Pb}^{2+}(\text{aq}) + 2\ \text{H}_2\text{O(l)}
Pour recharger complètement cette batterie, il faut \text{6} h avec un courant d'intensité égale à \text{7,8} A.
1. Préciser le rôle joué par l'accumulateur lors du démarrage. En déduire le transfert d'énergie.
2. Cette batterie est déchargée. Écrire les demi-équations aux électrodes lors de la charge de cette batterie.
3. Déterminer l'augmentation de la masse de l'électrode de plomb lors de la charge complète de l'accumulateur.
2. Cette batterie est déchargée. Écrire les demi-équations aux électrodes lors de la charge de cette batterie.
3. Déterminer l'augmentation de la masse de l'électrode de plomb lors de la charge complète de l'accumulateur.
Données
- Couples d'oxydoréduction : \text{PbO}_2 \text{(s)/Pb}^{2+}(\text{aq}) et \text{Pb}^{2+}\text{(aq)/Pb(s)}
- Masse molaire du plomb : M(\text{Pb}) = 207{,}2 g·mol‑1
- Constante de Faraday : F = 9{,}65 \times 10^4 C·mol‑1
Histoire des sciences

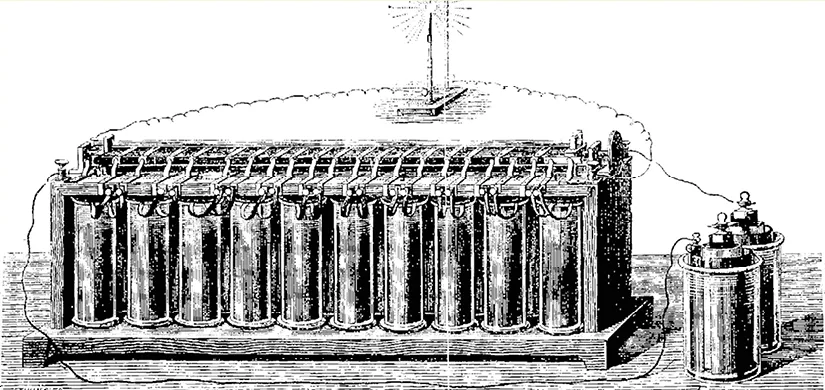
En 1859, le physicien-chimiste Gaston Planté met au point la première batterie électrique rechargeable. Sa batterie repose sur une réaction d'oxydoréduction impliquant du plomb, plongé dans un électrolyte d'acide sulfurique.
Ses travaux ont notamment permis le développement des batteries le siècle suivant, dont la plupart reposent encore aujourd'hui sur ce principe.
À noter : la première voiture à moteur électrique, la Jamais contente, était pourvu de ce type de batterie pour alimenter son moteur. Elle est la première voiture a avoir atteint la vitesse de \text{100} km·h‑1 en 1899, supplantant les précédents exploits réalisés avec des moteurs à combustion interne.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
AAccumulateur au lithium
✔ RAI/ANA : Modéliser une transformation
✔ APP : Extraire l'information utile
Made in Korea, assembled in China
3,8 V - 1900 mA·h
✔ APP : Extraire l'information utile
Il existe plusieurs types de batterie reposant sur l'élément lithium. Le plus commun est le type Li‑Ion qui repose sur la migration d'ions lithium \mathrm{Li}^{+} entre une électrode de graphite et une électrode de dioxyde de cobalt. Les deux électrodes baignent dans un électrolyte constitué d'un sel d'hexafluorophosphate de lithium \left(\mathrm{Li}^{+}(\mathrm{sa})~; \mathrm{PF}_{6}^{-}(\mathrm{sa})\right) dissout dans un solvant aprotique. La mention \mathrm{sa} désigne le fait que les ions sont dissous dans ce solvant.
L'ion \mathrm{Li}^{+}(\mathrm{sa}) a plus d'affinité avec le dioxyde de cobalt \mathrm{CoO}_{2}(\mathrm{~s}) qu'avec le graphite \mathrm{C}_{6}(\mathrm{~s}) ce qui signifie qu'il migre spontanément du graphite vers le dioxyde de cobalt. Il se produit alors les demi‑réactions suivantes :
L'ion \mathrm{Li}^{+}(\mathrm{sa}) a plus d'affinité avec le dioxyde de cobalt \mathrm{CoO}_{2}(\mathrm{~s}) qu'avec le graphite \mathrm{C}_{6}(\mathrm{~s}) ce qui signifie qu'il migre spontanément du graphite vers le dioxyde de cobalt. Il se produit alors les demi‑réactions suivantes :
- Sur l'électrode de graphite :
\mathrm{LiC}_{6}(\mathrm{~s}) \rightarrow \mathrm{C}_{6}(\mathrm{~s})+\mathrm{Li}^{+}(\mathrm{sa})+\mathrm{e}^{-} - Sur l'électrode de cobalt :
\mathrm{CoO}_{2}(\mathrm{~s})+\mathrm{Li}^{+}(\mathrm{sa})+\mathrm{e}^{-} \rightarrow \mathrm{LiCoO}_{2}(\mathrm{~s})
1. Les demi‑réactions présentées ont‑elle lieu lors de la charge ou de la décharge ?
2. Écrire l'équation globale de la réaction ayant lieu lors de la charge et celle lors de la décharge.
3. Calculer la masse de lithium échangée lors d'une charge ou d'une décharge complète.
4. Calculer la durée de la charge.
2. Écrire l'équation globale de la réaction ayant lieu lors de la charge et celle lors de la décharge.
3. Calculer la masse de lithium échangée lors d'une charge ou d'une décharge complète.
4. Calculer la durée de la charge.
Données
- Constante de Faraday : F = 9{,}65 \times 10^4 C·mol-1
Doc. 1
Caractéristiques de la batterie
Li‑Ion BatteryMade in Korea, assembled in China
3,8 V - 1900 mA·h
Doc. 2
Caractéristiques du chargeur
Charger EP800
Input : 100 - 240 V AC 50‑60 Hz 150 mA
Output : 5,0 V DC 850 mA
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
BBijou en or plaqué
✔ REA : Appliquer une formule
On souhaite réaliser le plaquage or d'un bijou en laiton. L'électrolyseur utilise une électrode de platine baignant dans une solution de chlorure d'or \left(\mathrm{Au}^{3+}(\mathrm{aq}) ; 3 ~\mathrm{Cl}^{-(\mathrm{aq}))}\right). Le courant de l'électrolyseur est de 800 mA. Le bijou constitue la deuxième électrode.
1. Écrire la demi‑équation associée au couple \mathrm{Au}^{3+}(\mathrm{aq}) / \mathrm{Au}(\mathrm{s}) qui se produit au niveau de la cathode.
2. Combien de temps doit‑on attendre pour déposer 100 mg d'or ?
On souhaite réaliser le plaquage or d'un bijou en laiton. L'électrolyseur utilise une électrode de platine baignant dans une solution de chlorure d'or \left(\mathrm{Au}^{3+}(\mathrm{aq}) ; 3 ~\mathrm{Cl}^{-(\mathrm{aq}))}\right). Le courant de l'électrolyseur est de 800 mA. Le bijou constitue la deuxième électrode.
1. Écrire la demi‑équation associée au couple \mathrm{Au}^{3+}(\mathrm{aq}) / \mathrm{Au}(\mathrm{s}) qui se produit au niveau de la cathode.
2. Combien de temps doit‑on attendre pour déposer 100 mg d'or ?
Données
- Constante de Faraday : F = 9{,}65 \times 10^4 C·mol-1
- Masse molaire de l'or : M = 197 g·mol-1
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

