Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Énoncé
Le but de cet exercice est d'étudier quelques propriétés des acides aminés alanine et aspartique, puis de comprendre la formation d'une liaison peptidique entre eux.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Acides aminés dans les larmes
Le lysozyme est une protéine présente dans les larmes. Elle est composée d'une chaîne d'une centaine d'acides aminés, dont la séquence Ala-Asp-Ala. Cette molécule a une activité antibactérienne, mais forme un voile blanc sur les lentilles de contact entraînant des sensations de brûlure ou des démangeaisons oculaires. Un entretien des lentilles par un produit de nettoyage est indispensable pour déprotéiner la lentille.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 3Synthèse de Strecker des acides aminés

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 2Formules semi-développées
La formule semi-développée de l'alanine, notée Ala est :

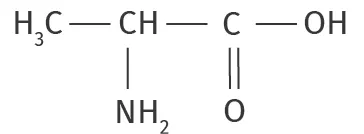
La formule semi-développée de l'acide aspartique, noté Asp est la suivante :

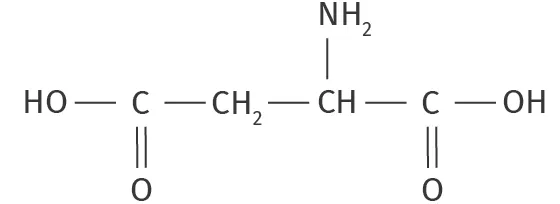
L'acide aspartique est un triacide. Les formes acides et basiques sont notées de façon simplifiée \text{AspH}_3, \text{AspH}^-_2 , \text{AspH}^{2-} et \text{Asp}^{3-}.

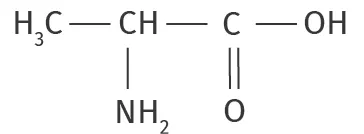
La formule semi-développée de l'acide aspartique, noté Asp est la suivante :


L'acide aspartique est un triacide. Les formes acides et basiques sont notées de façon simplifiée \text{AspH}_3, \text{AspH}^-_2 , \text{AspH}^{2-} et \text{Asp}^{3-}.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 4Lentilles de contact à nettoyer


Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- \textbf{p}\bm K_\textbf{A} du couple \textbf{AspH}_\bold{3}\textbf{(aq)}/\textbf{AspH}^-_\bold{2}\textbf{(aq)} : \text{p}K_{\text{A1}} = 2{,}0
- \textbf{p}\bm K_\textbf{A} du couple \textbf{AspH}^-_\bold{2}\textbf{(aq)}/\textbf{AspH}^\bold{2-}\textbf{(aq)} : \text{p}K_{\text{A2}} = 3{,}9
- \textbf{p}\bm K_\textbf{A} du couple \textbf{AspH}^\bold{2-}\textbf{(aq)}/ \textbf{AspH}^\bold{3-}\textbf{(aq)} : \text{p}K_{\text{A3}} = 9{,}8
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
1
À propos de l'acide aspartique
1.1 Écrire la formule topologique de l'acide aspartique.
1.2 Schématiser le diagramme de prédominance incluant les différentes formes acide-base de l'acide aspartique.
Cliquez pour accéder à une zone de dessin
1.3 Préciser quelle est la forme prédominante à \text{pH} = 7.
2
À propos de l'alanine
2.1 Écrire la formule topologique de l'alanine.
2.2 Préciser à quel type de réaction chimique appartiennent les étapes 1 et 2 de la synthèse de Strecker.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 5Protéines et liaison peptidique
Un peptide est un enchaînement de plusieurs acides aminés. Si un grand nombre (plus d'une dizaine) d'acides aminés sont reliés entre eux, la macromolécule est appelée protéine.
Les acides aminés sont reliés entre eux par une liaison peptidique formée par réaction entre le groupe amine et le groupe carboxyle.

Le nom d'un dipeptide renseigne sur sa structure. Sa dénomination commence par l'acide aminé dont le groupe caractéristique carboxyle a réagi, suivi par l'acide aminé dont le groupe amine a réagi. Ainsi, pour le dipeptide noté Cys-Gly, le groupe carboxyle de la cystéine a réagi avec le groupe amine de la glycine.
Les acides aminés sont reliés entre eux par une liaison peptidique formée par réaction entre le groupe amine et le groupe carboxyle.

Le nom d'un dipeptide renseigne sur sa structure. Sa dénomination commence par l'acide aminé dont le groupe caractéristique carboxyle a réagi, suivi par l'acide aminé dont le groupe amine a réagi. Ainsi, pour le dipeptide noté Cys-Gly, le groupe carboxyle de la cystéine a réagi avec le groupe amine de la glycine.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- Couples d'oxydoréduction : \text{H}_2\text{O}_2(\text{aq})/\text{H}_2\text{O} \text{(l)} et \text{O}_2\text{(g)/H}_2\text{O}_2\text{(aq)}
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 6Nettoyage de lentilles de contact
Les lentilles de contact doivent être nettoyées tous les jours. L'un des systèmes existants met en œuvre une réaction d'oxydoréduction du peroxyde d'hydrogène \text{H}_2\text{O}_2 \text{(aq)}. On place les lentilles dans un étui et l'on verse un peu de solution de peroxyde d'hydrogène, appelée eau oxygénée. Un disque de platine catalyse la réaction de décomposition de \text{H}_2\text{O}_2 \text{(aq)} en dioxygène \text{O}_2 \text{(aq)} et en eau \text{H}_2\text{O} \text{(l)}.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 7Eau oxygénée


L'eau oxygénée est une solution aqueuse de peroxyde d'hydrogène.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
3
Formation du dipeptide Ala-Asp
3.1 Reproduire les formules semi-développées de l'alanine et de l'acide aspartique, puis entourer en rouge les groupes caractéristiques sur les formules de ces deux acides aminés devant réagir pour former le dipeptide Ala-Asp.
3.2 Entourer en vert les groupes caractéristiques devant être protégés lors de cette synthèse. Expliquer ce qui se produirait si cette protection n'était pas réalisée.
Cliquez pour accéder à une zone de dessin
3.2 Entourer en vert les groupes caractéristiques devant être protégés lors de cette synthèse. Expliquer ce qui se produirait si cette protection n'était pas réalisée.
3.3 Schématiser les molécules d'alanine et d'acide aspartique avec leur groupe de protection symbolisé par la lettre P, puis faire de même pour la molécule obtenue.
3.4 Préciser le nom de l'étape qu'il reste à réaliser pour obtenir le dipeptide voulu.
3.5 Expliquer les étapes pour former ensuite la liaison entre le dipeptide Ala-Asp et l'acide aminé Ala.
Cliquez pour accéder à une zone de dessin
3.4 Préciser le nom de l'étape qu'il reste à réaliser pour obtenir le dipeptide voulu.
3.5 Expliquer les étapes pour former ensuite la liaison entre le dipeptide Ala-Asp et l'acide aminé Ala.
4
Nettoyage des lentilles de contact
4.1 Écrire les demi-équations correspondant aux couples donnés. En déduire la réaction de décomposition du peroxyde d'hydrogène.
4.2 Préciser le rôle joué par le disque de platine.
4.3 Décrire ce que l'on observe à la surface de ce disque de platine au cours de la réaction.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

