Chapitre 7
Exercices
Pour s'échauffer - Pour commencer
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
| Pour commencer | Différenciation | Pour s'entraîner | |
|---|---|---|---|
| Identifier le sens des transferts d'énergie : | |||
| Savoir écrire une équation pour un changement d'état : | |||
| Utiliser correctement les termes exothermique et endothermique : | |||
| Connaître et utiliser la formule de l'énergie transférée : |
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Pour s'échauffer
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
ALa paraffine
La paraffine, sert a la fabrication des bougies. Sa température de fusion est de 52 °C.
Indiquer son état physique à –10 °C, 45 °C et 60 °C.
Indiquer son état physique à –10 °C, 45 °C et 60 °C.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
4Repérer les grandeurs et unités
Rappeler la formule permettant de calculer la quantité d'énergie transférée au cours d'un changement d'état. Préciser toutes les grandeurs et les unités.Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
5Liquéfaction
Décrire le phénomène de liquéfaction du point de vue des échanges d'énergie.Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
6Chlorure de sodium
La fusion de sels de chlorure de sodium (NaCl) est réalisée dans certaines centrales solaires thermiques.Écrire l'équation de ce changement d'état.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
7Fusion
Décrire le phénomène de fusion du point de vue moléculaire.Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
8Fusion du chlorure de sodium (1)
On réalise la fusion de 10 kg de chlorure de sodium.Indiquer si ce sel capte ou libère de l'énergie.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
9Fusion du chlorure de sodium (2)
On réalise la fusion de 10 kg de chlorure de sodium.Calculer l'énergie nécéssaire.
Données
L_\text{fusion}\text{(NaCl)} = 481 \times 10^3 J·kg-1.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Pour commencer
Modélisation des transformations physiques
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
10Utiliser le modèle particulaire
✔ APP : Maîtriser le vocabulaire du cours
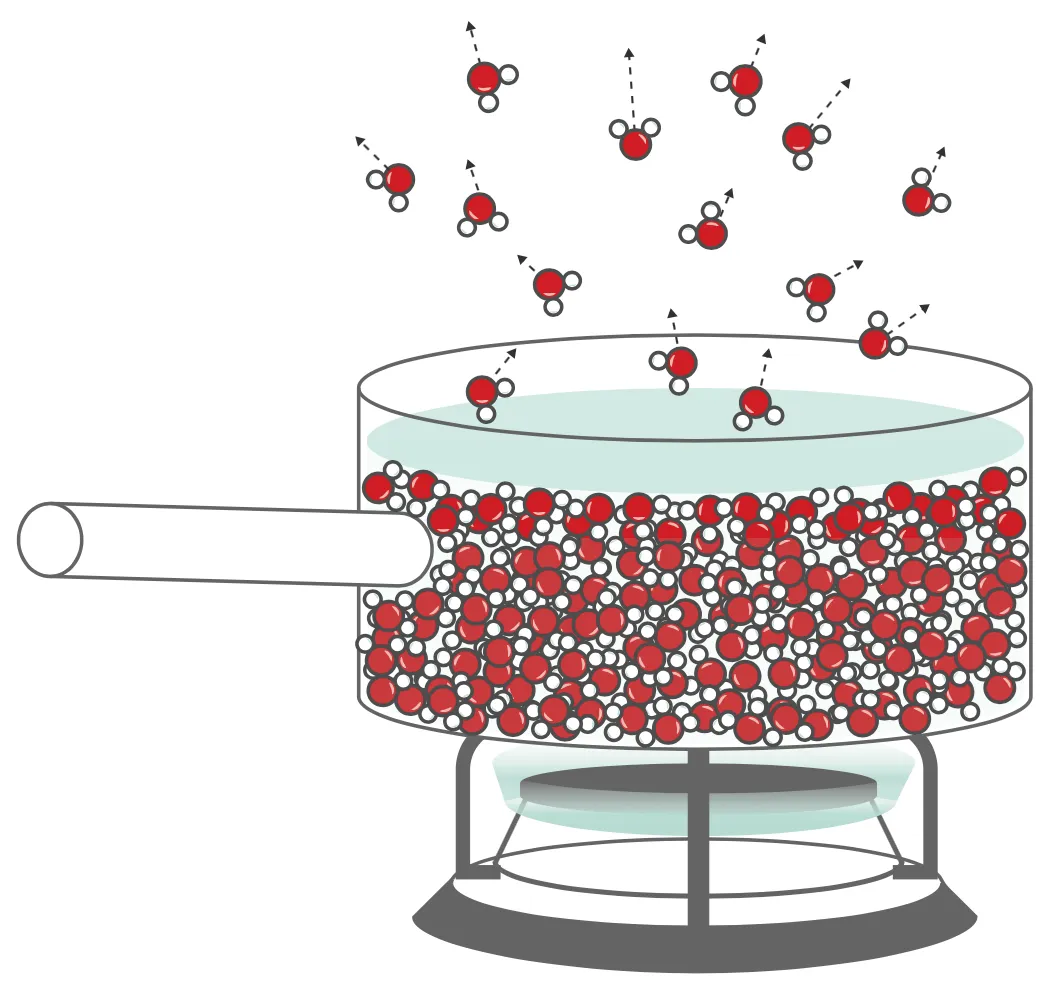
1.
Écrire l'équation de ce changement d'état et en préciser le nom.
2. Au cours de cette transformation physique, que peut-on dire de l'agitation des molécules et des liaisons entre les molécules ?
3. Faire une phrase complète en utilisant un vocabulaire rigoureux pour expliquer ce changement d'état à l'aide du modèle particulaire.
2. Au cours de cette transformation physique, que peut-on dire de l'agitation des molécules et des liaisons entre les molécules ?
3. Faire une phrase complète en utilisant un vocabulaire rigoureux pour expliquer ce changement d'état à l'aide du modèle particulaire.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
11Identifier l'état d'une espèce chimique
✔ MOD : Faire le lien entre les modèles microscopiques et les
grandeurs macroscopiquesSous pression atmosphérique normale et à la température de 25 °C, l'éthane est gazeux alors que l'éthanol est liquide.
1.
Quel est le composé le plus désordonné à 25 °C ?
2.
Dans quel composé les liaisons intermoléculaires sont-elles plus fortes à 25 °C ? Expliquer la réponse.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Les échanges d'énergie
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
12Calculer une énergie de changement d'état
✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie✔ MATH : Pratiquer le calcul numérique
De l'éther versé sur la peau procure une sensation de froid.
1. Expliquer ce phénomène (voir activité 1).
1. Expliquer ce phénomène (voir activité 1).
2.
Si la masse d'éther était de 5,0 g, calculer la quantité d'énergie transférée par la peau lors de ce changement d'état.
Température d'ébullition de l'éther : 35 °C ;
Énergie massique de vaporisation de l'éther : 376,5 kJ·kg-1.
Données
Température d'ébullition de l'éther : 35 °C ;
Énergie massique de vaporisation de l'éther : 376,5 kJ·kg-1.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
13Les comètes
✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie✔ MATH : Pratiquer le calcul littéral et le calcul numérique : puissances de 10


Du fait de leur longue orbite, parfois éloignée (au-delà des dernières planètes géantes), ces objets se trouvent loin de toute source de chaleur. Ils sont donc très froids et sous forme solide.
Lorsqu'une comète se rapproche du Soleil, les glaces se subliment et entraînent l'éjection de gaz et de poussières. Ce sont ces poussières qu'il est alors possible d'observer depuis la Terre car elles diffusent la lumière solaire et forment la chevelure de la comète.
1.
Écrire l'équation de changement d'état de l'eau au cours de la sublimation.
2. Cette transformation est-elle exothermique ou endothermique ? Justifier la réponse à l'aide du texte.
3. Calculer l'énergie nécessaire à fournir pour effectuer la sublimation d'un volume V = 3\text{,}5 \times 10^4 m3 de glace.
Masse volumique de l'eau solide : \rho = 917 kg·m3 ;
Énergie de changement d'état pour la sublimation de l'eau : L_\text{sublimation}\text{(eau)}= 2 \,837 kJ·kg-1.
2. Cette transformation est-elle exothermique ou endothermique ? Justifier la réponse à l'aide du texte.
3. Calculer l'énergie nécessaire à fournir pour effectuer la sublimation d'un volume V = 3\text{,}5 \times 10^4 m3 de glace.
Données
Masse volumique de l'eau solide : \rho = 917 kg·m3 ;
Énergie de changement d'état pour la sublimation de l'eau : L_\text{sublimation}\text{(eau)}= 2 \,837 kJ·kg-1.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Pour plus d'informations sur les comètes et leur chevelure, consultez le site !
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
14La lyophilisation
✔ APP : Faire un brouillon✔ MOD : Modéliser une transformation physique
La lyophilisation est un procédé de conservation d'un corps très utilisée en agroalimentaire.
Ce procédé met en jeu plusieurs étapes :
- la congélation du composé ;
- l'abaissement de pression dans l'enceinte de l'appareil.
Lors de cette deuxième phase, l'eau solide dans le composé passe à l'état de gaz. Le composé est ainsi presque déshydraté et pourra être conservé (c'est le cas du café soluble).
La congélation constitue l'étape critique. Si les cristaux de glace sont gros, après le passage à l'état gazeux, ils disparaissent en laissant la place à de gros pores dans le composé. Le composé risque alors de ne pas retrouver ces propriétés une fois réhydraté.


La congélation constitue l'étape critique. Si les cristaux de glace sont gros, après le passage à l'état gazeux, ils disparaissent en laissant la place à de gros pores dans le composé. Le composé risque alors de ne pas retrouver ces propriétés une fois réhydraté.


1.
Au brouillon, indiquer l'état physique de l'eau au cours des différentes étapes ainsi que le nom des changements d'état physique qu'elle subit.
2. Écrire alors les équations des changements d'état subis par l'eau.
3. Préciser le sens des transferts thermiques.
4. Que peut-on dire du solide formé à la fin de la première étape ? Expliquer la réponse par une modélisation de ce changement d'état au niveau microscopique.
2. Écrire alors les équations des changements d'état subis par l'eau.
3. Préciser le sens des transferts thermiques.
4. Que peut-on dire du solide formé à la fin de la première étape ? Expliquer la réponse par une modélisation de ce changement d'état au niveau microscopique.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
15L'éthanol
✔ MATH : Pratiquer le calcul numérique : puissances de 10
L'éthanol est liquide à température ambiante (sa température de vaporisation est de 79 °C).
1. L'éthanol reçoit-il ou cède-t-il de l'énergie thermique lors de la vaporisation ?
2. Cette transformation est-elle exothermique ou endothermique ?
1. L'éthanol reçoit-il ou cède-t-il de l'énergie thermique lors de la vaporisation ?
2. Cette transformation est-elle exothermique ou endothermique ?
3.
Calculer l'énergie transférée pour réaliser la vaporisation de 200 g d'éthanol à 79 °C en précisant si le système reçoit ou libère de l'énergie.
L_\text{vaporisation}\text{(éthanol)}= 855 kJ·kg-1.
Données
L_\text{vaporisation}\text{(éthanol)}= 855 kJ·kg-1.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
16L'acide acétique
✔ COM : Associer les bonnes unités aux grandeurs physiques et
faire des conversions
Le vinaigre contient de l'acide acétique dilué. Les températures de changement d'état de l'acide acétique pur sont \theta_\text{fusion} = 17 °C et \theta_\text{vaporisation} = 118 °C.
1. Quel est l'état physique de l'acide acétique à température ambiante ?
2. Calculer l'énergie transférée pour réaliser la vaporisation de 250 mL d'acide acétique à 118 °C.
Le vinaigre contient de l'acide acétique dilué. Les températures de changement d'état de l'acide acétique pur sont \theta_\text{fusion} = 17 °C et \theta_\text{vaporisation} = 118 °C.
1. Quel est l'état physique de l'acide acétique à température ambiante ?
2. Calculer l'énergie transférée pour réaliser la vaporisation de 250 mL d'acide acétique à 118 °C.
3.
Calculer l'énergie transférée pour réaliser la solidification de 250 mL d'acide acétique à 17 °C.
4. Préciser si ces réactions sont exothermiques ou endothermiques.
4. Préciser si ces réactions sont exothermiques ou endothermiques.
Données
- L_\text{vaporisation}\text{(acide acétique)}= 395 kJ·kg-1 ;
- L_\text{solidification}\text{(acide acétique)}= - 195\text{,}5 kJ·kg-1 ;
- Masse volumique de l'acide acétique : \rho = 1\text{,}049 g·mL-1.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
BLes MCP
✔ APP : Faire un brouillon comprenant un schéma, données et notions
✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie
Les Matériaux à Changement de Phase (MCP) ont pour particularité de pouvoir stocker de l'énergie lorsqu'ils changent d'état physique. Insérer dans des petites capsules en polymère, dans de la peinture, ils sont capables d'assurer un meilleur confort thermique dans la maison.
Ainsi, lorsque la température diminue, le matériau, dans la capsule, se solidifie et cette réaction dégage de la chaleur. À l'inverse, une élévation de température ramènera le matériau à son état liquide en consommant de l'énergie. Ainsi une couche de 15 millimètres d'un enduit MCP apporte la même inertie thermique que 2 ou 3 centimètres de béton.

✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie
Les Matériaux à Changement de Phase (MCP) ont pour particularité de pouvoir stocker de l'énergie lorsqu'ils changent d'état physique. Insérer dans des petites capsules en polymère, dans de la peinture, ils sont capables d'assurer un meilleur confort thermique dans la maison.
Ainsi, lorsque la température diminue, le matériau, dans la capsule, se solidifie et cette réaction dégage de la chaleur. À l'inverse, une élévation de température ramènera le matériau à son état liquide en consommant de l'énergie. Ainsi une couche de 15 millimètres d'un enduit MCP apporte la même inertie thermique que 2 ou 3 centimètres de béton.

1.
Sur un brouillon, récolter toutes les informations concernant les MCP. Organiser les à l'aide d'un schéma.
2. Écrire les deux équations de changement d'état indiquées dans le le texte et préciser si les transformations sont exothermiques ou endothermiques.
3. Précisez le système avec lequel le MCP échange de l'énergie.
4. Justifier rigoureusement par des considérations énergétiques la phrase : « assurer un meilleur confort thermique dans la maison ».
Cliquez pour accéder à une zone de dessin
2. Écrire les deux équations de changement d'état indiquées dans le le texte et préciser si les transformations sont exothermiques ou endothermiques.
3. Précisez le système avec lequel le MCP échange de l'énergie.
4. Justifier rigoureusement par des considérations énergétiques la phrase : « assurer un meilleur confort thermique dans la maison ».
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Une notion, trois exercicesDifférenciation
Savoir-faire : Identifier le sens des transferts d'énergie.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
La pompe à chaleur géothermique (PAC)
Pour les exercices

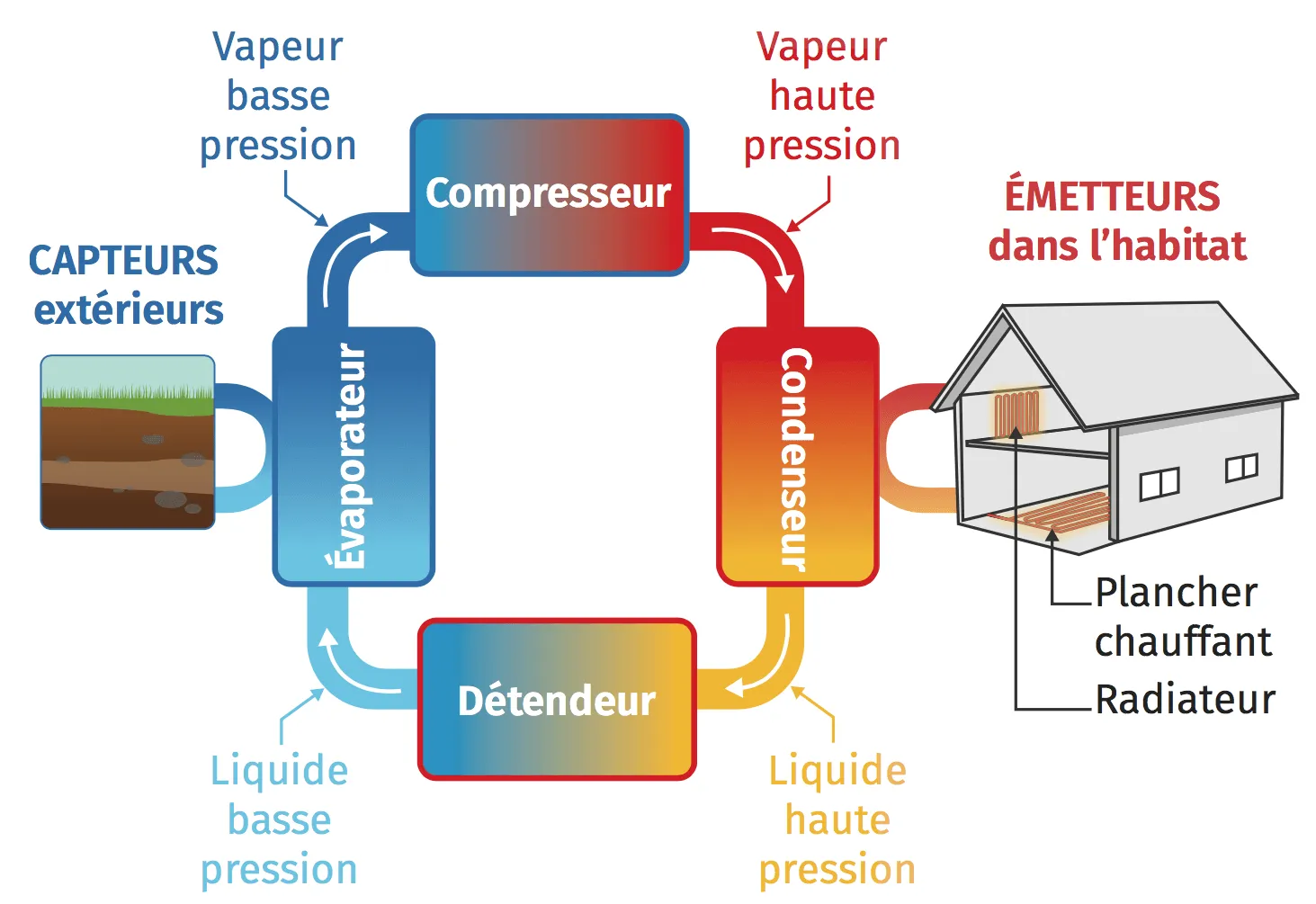
17
à 19
.

La PAC géothermique puise son énergie du sol pour délivrer un chauffage et une eau chaude très économes. Elle permet ainsi de valoriser l'énergie renouvelable en l'absorbant à l'extérieur puis en la restituant à l'intérieur de l'habitation par l'intermédiaire d'un circuit de distribution (plancher chauffant, réseau de radiateurs, ventilo-convecteurs). Pour cela, un fluide frigorifique circule dans un circuit fermé.
- Le fluide frigorigène présent dans ce circuit est amené de l'état liquide à l'état gazeux dans l'évaporateur, permettant ainsi de récupérer la chaleur du sol ou du puits.
- Le compresseur augmente la pression du fluide, ce qui augmente aussi sa température.
- Dans le condenseur, le fluide transmet la chaleur au circuit de chauffage tout en passant à l'état liquide.
- Le fluide frigorigène traverse le détendeur thermostatique et se retrouve à l'état initial en basse pression et basse température, avant de retourner à l'évaporateur.
Extrait de
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
17L'évaporateur et le condenseur
✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie
1.
Numéroter sur le schéma les différentes parties de la pompe à chaleur.
2. Faire un schéma à l'échelle moléculaire expliquant le phénomène mis en jeu dans l'évaporateur.
2. Faire un schéma à l'échelle moléculaire expliquant le phénomène mis en jeu dans l'évaporateur.
Cliquez pour accéder à une zone de dessin
3.
Justifier alors la phrase « l'évaporateur, permettant ainsi de récupérer la chaleur du sol ».
4. Répondre aux questions 2 et 3 pour le condenseur.
5. Expliquer le principe de chauffage par géothermie.
4. Répondre aux questions 2 et 3 pour le condenseur.
Cliquez pour accéder à une zone de dessin
5. Expliquer le principe de chauffage par géothermie.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
18Le fluide frigorigène
✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie1. Quel est le rôle du fluide frigorigène ?
2. Dans quelle partie du système absorbe-t-il de l'énergie ? Expliquer le phénomène physique.
3. Dans quelle partie du système libère-t-il de l'énergie ? Expliquer le phénomène physique.
4. Expliquer alors le principe de chauffage par géothermie.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
19L'évaporateur et le condenseur
✔ MOD : Utiliser de façon rigoureuse le modèle de l'énergie1. Identifier les parties de la pompe où des changements d'état physique ont lieu.
2. Préciser dans chaque cas si ces transformations sont exothermiques ou endothermiques.
3. Indiquer toutes les différences que présente le fluide frigorigène entre l'entrée et la sortie du compresseur, notamment pour ce qui concerne l'énergie qu'il contient.
4. Les pompes à chaleur sont dites dithermes. Expliquer pourquoi.
5. Expliquer le principe de chauffage par géothermie.
