Fiche méthode D
Compétences
Exclusivité numérique
Analyser : Lien microscopique/macroscopique
Télécharger la fiche méthode au format pdf .Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
A Les mondes macroscopique et microscopique
❯
Le monde macroscopique est constitué de tout ce qui peut se mesurer et s'observer à notre échelle. La taille des objets décrits varie du millimètre à quelques dizaines de mètre.
❯ Le monde microscopique est constitué de ce qui est trop petit pour être observé directement, les objets sont donc décrits par des modèles chimiques. Attention, le monde microscopique de la chimie est plus petit que celui de la SVT par exemple. En chimie, il décrit des objets de l'ordre du nanomètre (10^{-9} m), on pourrait parler de monde nanoscopique. Cela exclut toute observation possible au microscope optique.
❯ Le rôle de la chimie est de faire ce lien entre ces deux mondes. Les modèles microscopiques sont utilisés pour expliquer les propriétés macroscopiques de la matière.
❯ Le monde microscopique est constitué de ce qui est trop petit pour être observé directement, les objets sont donc décrits par des modèles chimiques. Attention, le monde microscopique de la chimie est plus petit que celui de la SVT par exemple. En chimie, il décrit des objets de l'ordre du nanomètre (10^{-9} m), on pourrait parler de monde nanoscopique. Cela exclut toute observation possible au microscope optique.
❯ Le rôle de la chimie est de faire ce lien entre ces deux mondes. Les modèles microscopiques sont utilisés pour expliquer les propriétés macroscopiques de la matière.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1 Eau décrite au niveau
macroscopique


Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
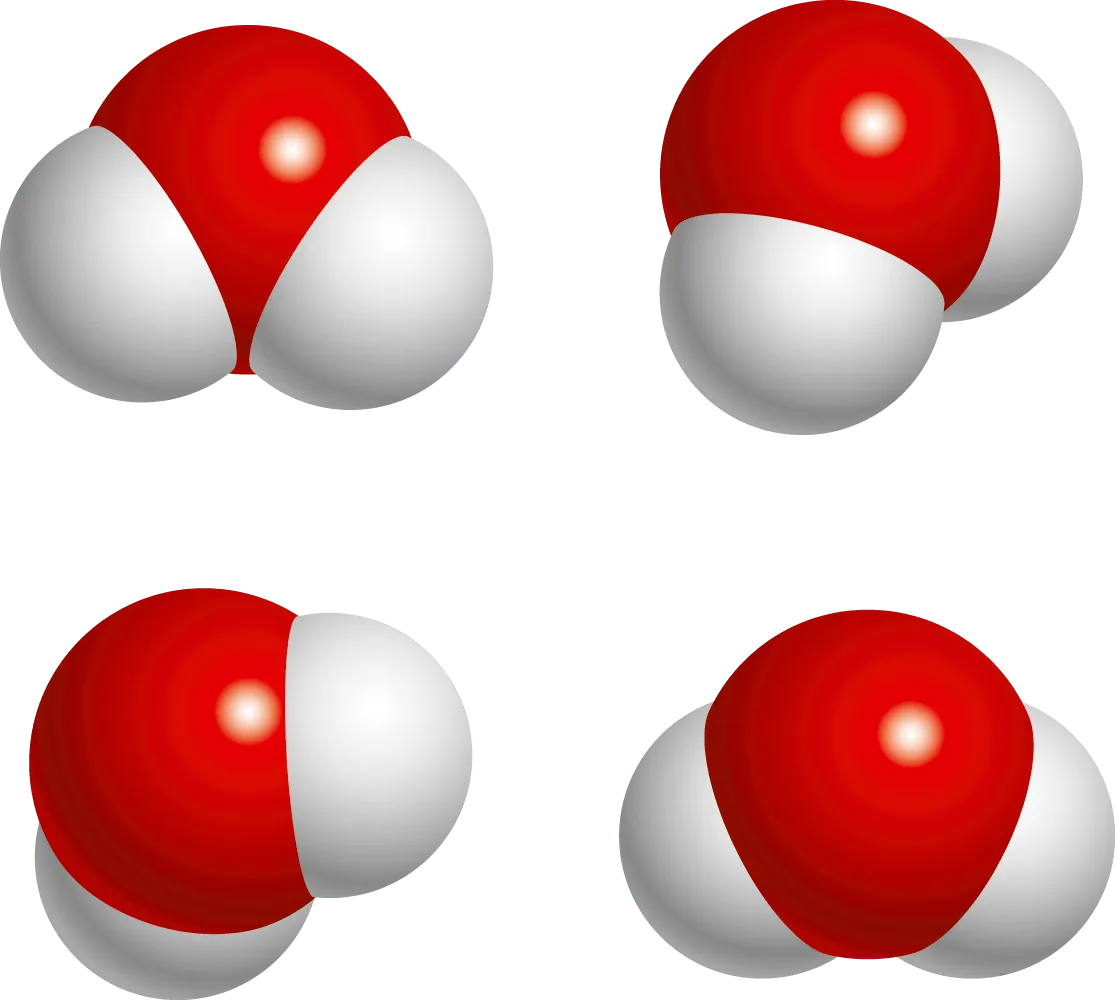
Doc. 2 Eau décrite au niveau microscopique

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
B Le modèle particulaire de la matière
❯ À l'échelle microscopique, la matière est constituée de particules. Ces particules ont des propriétés propres et interagissent les unes avec les autres. Les exercices permettent d'étudier une ou plusieurs particules à la fois (de l'ordre d'une dizaine d'éléments).
❯ À l'échelle macroscopique, les particules sont considérées en beaucoup plus grand nombre. L'ordre de grandeur du nombre de molécules qu'on considère est de 10^{23}, soit l'ordre de grandeur du nombre d'Avogadro N_\text{A}.
❯ Pour passer d'une échelle à l'autre, on utilise la notion de quantité dematière, exprimée en mole (mol).
❯ À l'échelle macroscopique, les particules sont considérées en beaucoup plus grand nombre. L'ordre de grandeur du nombre de molécules qu'on considère est de 10^{23}, soit l'ordre de grandeur du nombre d'Avogadro N_\text{A}.
❯ Pour passer d'une échelle à l'autre, on utilise la notion de quantité dematière, exprimée en mole (mol).
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
C Lien microscopique/macroscopique
Pour rédiger un exercice qualitatif de chimie, il faut donc commencer par identifier dans l'énoncé ce qui est de l'ordre du microscopique. Puis, utiliser un ou plusieurs des trois modèles à disposition en s'appuyant sur des schémas pour expliquer ce qui se passe au niveau microscopique. Enfin, conclure en faisant le lien vers les conséquences du phénomène observé à l'échelle macroscopique.
| Échelle microscopique (modèles) | Modèle de l'atome (voir ) Modèle de Lewis (voir ) Modèle particulaire (voir et collège) |
| Propriétés et grandeurs physiques macroscopiques | Masse, volume, concentration Température de changement d'état, densité, masse volumique Mélange, corps pur, solution Caractéristiques physiques et chimiques de la matière |
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille
