Chapitre 2
Activité 2 - Activité expérimentale
90 min
Sérum physiologique
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Objectif : Exploiter la loi de Kohlrausch et citer son domaine de validité.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Problématique de l'activité
Le sérum physiologique est une solution de chlorure de sodium couramment utilisé dans les pharmacies familiales. Peu coûteux, il sert à nettoyer les yeux, le nez ou à laver les plaies.
Comment peut-on vérifier la concentration d'un sérum physiologique ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 1Loi de Kohlrausch
Pour des solutions suffisamment diluées, la conductivité \sigma de la solution s'exprime en fonction des concentrations des ions qu'elle contient. Pour une solution contenant deux types d'ions \text{X}_1\text{(aq)} et \text{X}_2\text{(aq)}
La conductivité molaire ionique \lambda est une caractéristique propre à l'ion considéré. Elle est constante à température donnée et traduit la contribution apportée par cet ion à la conductivité globale de la solution.
\sigma=\lambda_{1} \cdot\left[\mathrm{X}_{1}\right]+\lambda_{2} \cdot\left[\mathrm{X}_{2}\right]
\sigma : conductivité de la solution (S·m-1)
\lambda_1 et \lambda_2 : conductivités molaires ioniques de \text{X}_1\text{(aq)} et \text{X}_2\text{(aq)} (S·m2·mol-1)
[\text{X}_1] et [\text{X}_2] : concentrations de \text{X}_1\text{(aq)} et de \text{X}_2\text{(aq)} (mol·m-3)
\lambda_1 et \lambda_2 : conductivités molaires ioniques de \text{X}_1\text{(aq)} et \text{X}_2\text{(aq)} (S·m2·mol-1)
[\text{X}_1] et [\text{X}_2] : concentrations de \text{X}_1\text{(aq)} et de \text{X}_2\text{(aq)} (mol·m-3)
La conductivité molaire ionique \lambda est une caractéristique propre à l'ion considéré. Elle est constante à température donnée et traduit la contribution apportée par cet ion à la conductivité globale de la solution.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
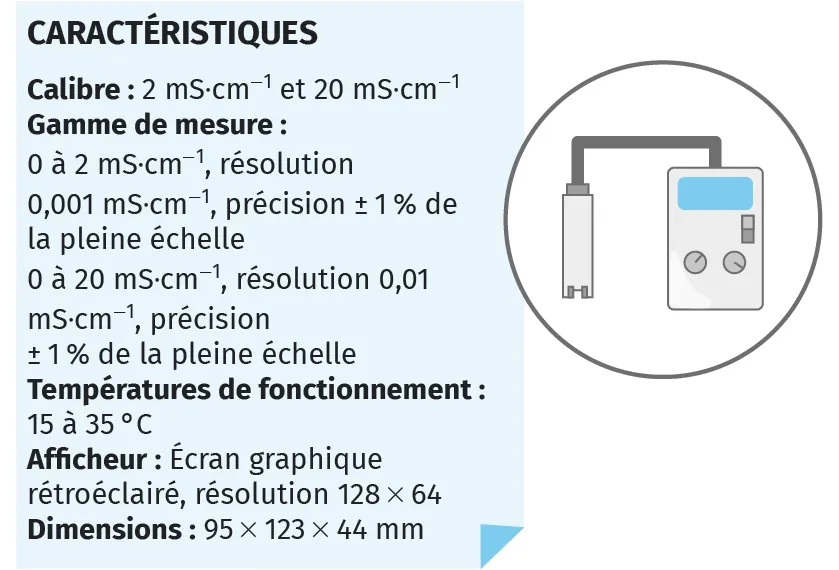
Doc. 2Caractéristiques du conductimètre

Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 3Matériel nécessaire
- Cinq fioles jaugées de 10{,}0 mL
- Solution de chlorure de sodium \text{S}_0 (\text{Na}^+\text{(aq)} ; \text{Cl}^-\text{(aq)}) de concentration en soluté apporté c_0 = 1{,}0 × 10^{-2} mol·L-1
- Sérum physiologique commercial à 0{,}9 %, dilué 20 fois
- Pipette graduée 10,0 mL
- Deux béchers
- Eau distillée
- Conductimètre
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- Conductivités molaires ioniques à 25 °C :
\lambda\left(\mathrm{Na}^{+}\right)=5{,}01 \times 10^{-3} S·m2·mol-1 et \lambda\left(\mathrm{Cl}^{-}\right)=7{,}63 \times 10^{-3} S·m2·mol-1 - Masse molaire du chlorure de sodium : M(\mathrm{NaCl})=58{,}4 g·mol-1
- Masse volumique du sérum physiologique : \rho_{\text {sérum }}=1,00 g·mL-1
- Expression du titre massique : t=\frac{m_{\text {soluté }}}{m_{\text {solution }}}
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Consultez
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Questions
Compétence(s)
VAL : Exploiter un ensemble de mesures
REA : Effectuer des mesures avec des capteurs
REA : Effectuer des mesures avec des capteurs
2. Réaliser quatre solutions étalons de concentration comprise entre 1{,}0 \times 10{^-3} mol·L-1et c_0 à partir de la solution \text{S}_0. Mesurer les conductivités \sigma de ces solutions.
3. Tracer la courbe d'étalonnage \sigma = f(c). Vérifier la proportionnalité entre ces grandeurs. 4. Mesurer la conductivité \sigma des cinq solutions. Proposer une relation simple entre la conductivité \sigma et la concentration c en chlorure de sodium apporté.
5. Comparer les résultats avec l'indication précisée dans le doc. 3.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Synthèse de l'activité
Rédiger un protocole permettant de retrouver la concentration d'une solution commerciale à l'aide de mesures de la conductivité de plusieurs solutions étalons.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

